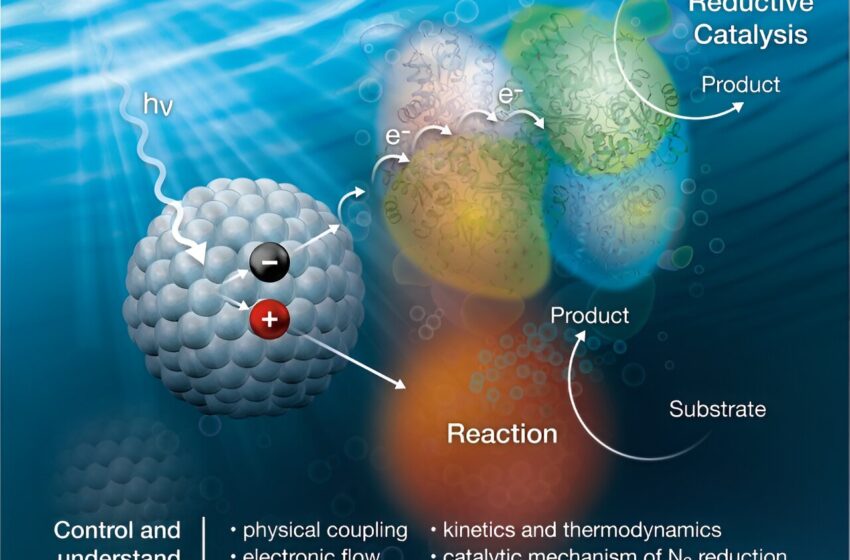
Alimenter les enzymes avec de la lumière pour produire de l’ammoniac
Les nanocristaux (à gauche) capturent la lumière (hv) puis transfèrent des électrons (e-) aux enzymes nitrogénases (en haut à droite) pour convertir le diazote (N2) en ammoniac (NH3). Une réaction sacrificielle (en bas à droite) complète le processus. Crédit : Alfred Hicks, National Renewable Energy Laboratory.
L’atmosphère terrestre contient de grandes quantités d’azote sous forme de gaz diazote (N2). Conversion de N2 à l’ammoniac (NH3) est essentiel à la fabrication des engrais nécessaires à l’agriculture.
Actuellement, la production d’ammoniac nécessite 2 % de l’énergie mondiale et génère d’importantes émissions de gaz à effet de serre. Dans la nature, l’enzyme nitrogénase peut catalyser la production d’ammoniac en utilisant l’énergie stockée dans l’adénosine triphosphate (ATP) pour déclencher la réaction.
L’ATP est une molécule naturelle présente dans toutes les formes de vie. Il est possible de remplacer l’ATP par l’énergie solaire pour un processus à faible consommation d’énergie qui ne produit pas de gaz à effet de serre.
Cependant, les chercheurs continuent de développer ces processus basés sur la lumière solaire.
Dans une recherche publiée dans Journal de la Société américaine de chimieLes scientifiques ont créé un biohybride unique qui associe des nanocristaux à la nitrogénase. Les nanocristaux utilisent la lumière du soleil pour transférer la charge aux enzymes et terminer la réaction. La recherche a identifié les propriétés des nanocristaux pour se lier à la nitrogénase, aidant les scientifiques à obtenir de nouvelles connaissances sur ce complexe NH3 réaction de production.
Cette approche biohybride utilise la lumière du soleil pour alimenter les réactions de conversion exigeantes en énergie qui peuvent atténuer la coproduction de gaz à effet de serre. L’approche standard pour produire de l’ammoniac est le procédé Haber-Bosch. Ce procédé produit environ 150 millions de tonnes métriques (MmT) d’ammoniac par an, mais nécessite de grandes quantités d’énergie et produit également environ 280 MmT de dioxyde de carbone (CO2).
Le nouveau procédé utilise la lumière du soleil pour catalyser le NH3 production sans génération de CO2C’est aussi une manière intéressante de produire du NH3 des engrais à proximité de l’endroit où ils seront utilisés, minimisant ainsi les émissions de CO2 émissions provenant du transport vers les fermes. Pour que ce processus devienne une réalité, il faut comprendre comment coupler la lumière du soleil pour déclencher la réaction.
Pour produire de l’ammoniac à l’aide de la lumière du soleil, les chercheurs ont développé un système biohybride composé de nanocristaux et de l’enzyme Mo-nitrogénase. Cette enzyme possède un groupe métallique unique, appelé cofacteur FeMo, qui nécessite huit électrons et huit protons pour réduire N2 à l’ammoniac.
Les chercheurs ont utilisé ce système nanocristal/enzyme pour déterminer comment diriger les électrons photogénérés vers le cofacteur FeMo et pour étudier le mécanisme associé. Pour que le système s’appuie sur la lumière, la nanoparticule et l’enzyme doivent être chimiquement compatibles et former un complexe réactionnel stable. Cette recherche a exploré comment fabriquer des nanoparticules qui se lient à l’enzyme.
Cette approche permet de comprendre comment ajuster synthétiquement les nanocristaux pour lier les enzymes et transférer la charge de manière sélective. Grâce à ces progrès, les chercheurs peuvent étudier le processus en détail. À l’état congelé, les intermédiaires de réaction du cofacteur FeMo peuvent être piégés et analysés en détail par des techniques de spectroscopie de résonance paramagnétique électronique.
Cette base technique permet aux chercheurs d’identifier les intermédiaires de réaction, les énergies d’activation des étapes de réaction et l’évolution d’un modèle cinétique du N2 réaction de réduction.
Plus d’informations :
Gregory E. Vansuch et al., Le recuit cryogénique de complexes protéiques MoFe photoréduits à points quantiques CdS-nitrogenase révèle la stabilité cinétique de l’intermédiaire E4(2N2H), Journal de la Société américaine de chimie (2023). DOI: 10.1021/jacs.3c06832
Lauren M. Pellows et al., Les interactions électrostatiques à haute affinité favorisent la formation de complexes protéiques CdS Quantum Dot:Nitrogenase MoFe, Lettres Nano (2023). DOI: 10.1021/acs.nanolett.3c03205
Lauren M. Pellows et al., Piégeage à basse température des intermédiaires de réaction de réduction de N2 dans les complexes de points quantiques protéine MoFe–CdS de la nitrogénase, Journal de physique chimique (2023). DOI: 10.1063/5.0170405
Fourni par le ministère américain de l’Énergie
Citation: Alimenter les enzymes avec de la lumière pour produire de l’ammoniac (2024, 9 août) récupéré le 9 août 2024 à partir de
Ce document est soumis au droit d’auteur. En dehors de toute utilisation équitable à des fins d’étude ou de recherche privée, aucune partie ne peut être reproduite sans autorisation écrite. Le contenu est fourni à titre d’information uniquement.
