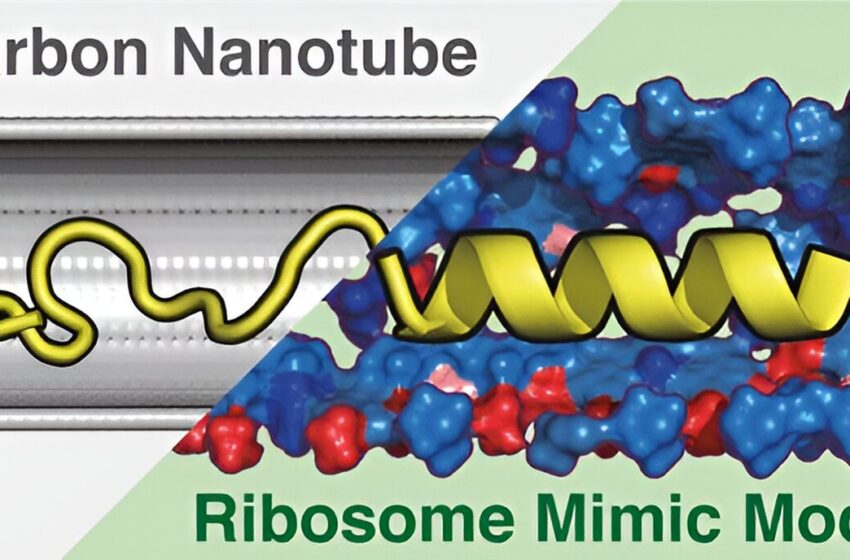
Un modèle de simulation montre l’impact du tunnel ribosomique sur les structures protéiques
Résumé graphique. Crédit : Journal d’information et de modélisation chimiques (2024). DOI: 10.1021/acs.jcim.4c00901
Des chercheurs de l’Université de Tsukuba ont développé un nouveau modèle qui simule l’environnement interne d’un ribosome, le site cellulaire de la synthèse des protéines. À l’aide de simulations informatiques, ils ont analysé les structures de diverses protéines au sein de ce modèle. Leurs résultats révèlent que les propriétés chimiques du tunnel du ribosome, par lequel passent les protéines nouvellement synthétisées, jouent un rôle crucial dans la formation des structures protéiques lors de la traduction.
Les protéines sont synthétisées par les ribosomes puis libérées par un canal tubulaire appelé tunnel ribosomique. Des études récentes suggèrent que certaines protéines commencent à former des structures tridimensionnelles (3D) fonctionnellement importantes alors qu’elles se trouvent encore à l’intérieur du tunnel ribosomique. Cependant, le mécanisme exact sous-jacent à ce processus reste mal compris.
Pour répondre à ces questions, des chercheurs de l’Université de Tsukuba ont analysé de manière exhaustive les structures 3D des tunnels ribosomiques rapportées à ce jour. L’étude est publiée dans la revue Journal d’information et de modélisation chimiques.
Sur la base de cette étude, ils ont développé un modèle cylindrique appelé modèle mimant l’environnement du ribosome (REMM), qui reproduit à la fois les diamètres intérieurs et les propriétés chimiques des tunnels du ribosome, caractéristiques clés du ribosome.
À titre de comparaison, ils ont également fabriqué un modèle de nanotube de carbone (CNT) classique – une molécule tubulaire uniquement composée d’atomes de carbone – qui reproduit uniquement le diamètre intérieur du tunnel tout en ignorant ses propriétés chimiques.
L’équipe a ensuite utilisé des simulations de dynamique moléculaire pour examiner les structures protéiques au sein de ces modèles. Les résultats ont révélé que le REMM reproduisait plus précisément les structures protéiques observées expérimentalement dans le tunnel du ribosome que le CNT.
De plus, la diversité chimique des REMM a été identifiée comme un facteur clé contribuant à leur capacité supérieure à répliquer des structures protéiques expérimentales. Un perfectionnement plus poussé des REMM devrait améliorer notre compréhension des conformations protéiques dans les cellules vivantes.
Plus d’informations :
Takunori Yasuda et al., L’environnement du tunnel ribosomique favorise la formation de l’hélice α lors du repliement cotraductionnel, Journal d’information et de modélisation chimiques (2024). DOI: 10.1021/acs.jcim.4c00901
Fourni par l’Université de Tsukuba
Citation:Un modèle de simulation montre l’impact du tunnel ribosomique sur les structures protéiques (2024, 28 août) récupéré le 28 août 2024 à partir de
Ce document est soumis au droit d’auteur. En dehors de toute utilisation équitable à des fins d’étude ou de recherche privée, aucune partie ne peut être reproduite sans autorisation écrite. Le contenu est fourni à titre d’information uniquement.
