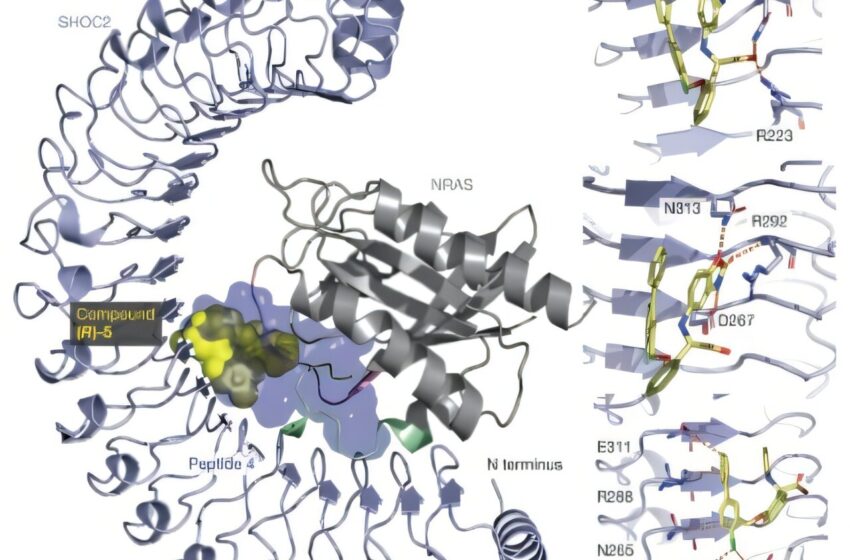
L’écran CRISPR à l’échelle du génome identifie une nouvelle cible dans le mélanome axé sur les NRAS
A) Représentation du SHOC2 lié au peptide 4 (surface violette légère; PDB: 9BTN), composé (R) -5 (sphères jaunes; PDB: 9BTP) et NRAS (Q61R) (gris; PDB: 9BTM). b) Le haut, le composé (R) -5 interagit avec R223 et Q269 via son acide carboxylique. Crédit: Nature (2025). Doi: 10.1038 / s41586-025-08931-1
Des chercheurs de Novartis Biomedical Research aux États-Unis et en Suisse ont identifié une cible moléculaire qui pourrait fournir une nouvelle voie thérapeutique pour les cancers entraînés par les mutations NRAS. Les résultats suggèrent que l’interférer avec des interactions protéiques spécifiques pourrait perturber les voies de signalisation associées à une prolifération cellulaire incontrôlée dans les tumeurs malignes dépourvues de traitements ciblés.
KRAS et NRAS sont des membres de la famille des gènes RAS, qui codent pour les protéines qui régulent la croissance et la division cellulaire par des voies de signalisation. Les mutations de ces gènes perturbent la signalisation normale, conduisant à l’oncogenèse. Les mutations du codon 12 dans les KRA sont courantes dans les tumeurs solides, tandis que les mutations du codon 61 dans les NRA sont principalement associées au mélanome.
Des thérapies ciblées ont été développées pour les mutations de KRAS (G12C) et de KRAS (G12D), mais des stratégies efficaces pour les cancers mutants NRAS restent insaisissables. Les mutations NRAS représentent 20 à 30% des cas de mélanome, ce qui représente un écart thérapeutique substantiel, en particulier compte tenu de l’absence de thérapies ciblées approuvées pour ce sous-ensemble.
Avec 50 000 nouveaux cas par an aux États-Unis et en Europe, le mélanome mutant NRAS continue de présenter un besoin clinique non satisfait. L’identification des dépendances moléculaires spécifiques associées à ces mutations pourrait révéler de nouvelles cibles thérapeutiques et éclairer les stratégies de traitement pour les tumeurs malignes axées sur les NRAS.
Dans l’étude, «ciblant l’interaction Shoc2 – Ras dans les cancers Ras-Mutant», publié dans Natureles chercheurs ont mené un écran CRISPR à l’échelle du génome pour identifier les dépendances génétiques associées aux mutations NRAS (Q61 *).
Des lignées cellulaires BA / F3 conçues pour exprimer des mutations KRAS et NRAS aux codons 12 et 61 ont été utilisées pour modéliser la dépendance oncogène RAS / MAPK en l’absence d’autres altérations génétiques.
Une bibliothèque Lenviral ARNm à l’échelle du génome a évalué les dépendances de croissance des lignées mutantes KRAS et NRAS dans des conditions contrôlées. Les dépendances sélectives des mutants et des isoformes ont ensuite été confirmées en utilisant des inhibiteurs de petite molécule spécifiques à KRAS (G12C) et KRAS (G12D). Une analyse ultérieure s’est concentrée sur l’identification des vulnérabilités génétiques uniques aux mutants NRAS (Q61 *).
SHOC2 est devenu une dépendance significative dans les modèles NRAS (Q61 *) – mutants. Dans les lignées cellulaires BA / F3, le knockout SHOC2 médié par l’AGNA a conduit à une létalité cellulaire prononcée, avec des mutants NRAS (Q61 *) présentant une sensibilité accrue par rapport aux lignées mutantes de KRAS (G12 *).
Dans les modèles de xénogreffe de mélanome, l’épuisement de SHOC2 a entraîné une inhibition de la croissance tumorale comparable à celle observée après le knockdown NRAS, suggérant que le ciblage de SHOC2 pourrait perturber la signalisation MAPK dans les tumeurs malignes pilotées par NRAS.
L’analyse des modèles de xénogreffes de mélanome a en outre démontré que la déplétion de SHOC2 réduisait considérablement la croissance tumorale dans les paramètres mutants d’ANR (Q61 *). Une prolifération cellulaire réduite et une diminution de la signalisation MAPK ont été observées in vitro après le knockdown SHOC2, s’alignant avec les résultats in vivo.
Des études mécanistes ont confirmé que SHOC2 forme une interaction directe avec les NRAS (Q61R) et KRAS (Q61R), avec des affinités de liaison similaires. Les efforts d’optimisation structurelle ont conduit à l’identification de composés de petites molécules capables de lier le SHOC2 et de perturber l’interaction SHOC2 – RAS, avec un composé démontrant une inhibition dose-dépendante de la signalisation RAS / MAPK dans les cellules de mélanome mutantes d’ANR (Q61 *).
Le ciblage de SHOC2 dans le cancer de Mutant NRAS (Q61) présente une stratégie thérapeutique distincte du ciblage direct du RAS, empêchant potentiellement la signalisation des cellules cancéreuses par des perturbations d’interaction SHOC2 – ARS.
L’identification des liants à petite molécule à SHOC2 illustre son potentiel médicamenteux dans le mélanome axé sur le NRAS, avec des implications plus larges pour d’autres cancers de mutant Ras où SHOC2 régule la signalisation MAPK.
Plus d’informations:
Zachary J. Hausteman et al, ciblant l’interaction shoc2 – las dans les cancers ras-mutants, Nature (2025). Doi: 10.1038 / s41586-025-08931-1
Hugo Lavoie et al, bloquant un nœud clé dans la signalisation du cancer déverrouille le potentiel thérapeutique, Nature (2025). Doi: 10.1038 / d41586-025-01136-6
© 2025 Science X Réseau
Citation: L’écran CRISPR à l’échelle du génome identifie une nouvelle cible dans le mélanome axé sur le NRAS (2025, 12 mai) récupéré le 13 mai 2025 à partir de
Ce document est soumis au droit d’auteur. Outre toute émission équitable aux fins d’études privées ou de recherche, aucune pièce ne peut être reproduite sans l’autorisation écrite. Le contenu est fourni uniquement à des fins d’information.
