Le « dogme central » de la biologie pourrait-il induire en erreur les bio-ingénieurs ?
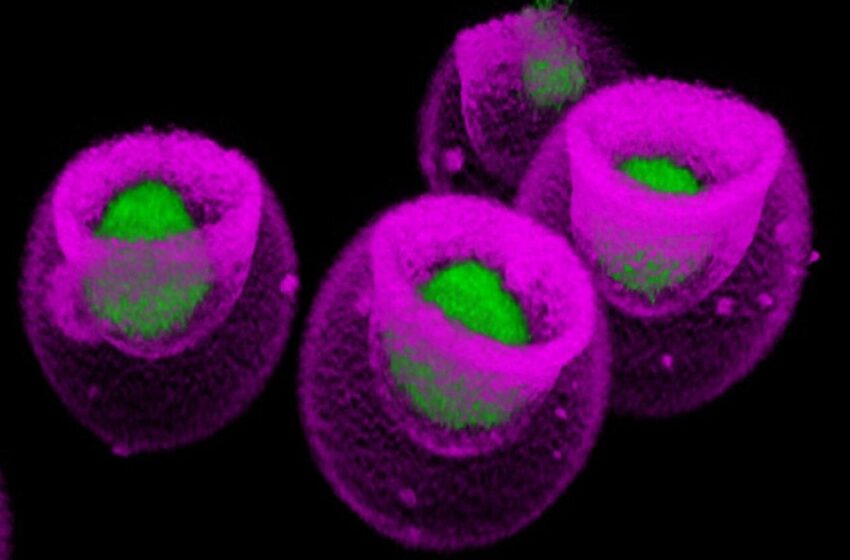
L’image microscopique confocale montre des cellules souches mésenchymateuses (vertes) capturées dans des nanovials (roses). La technologie nanoviale a été développée par Dino Di Carlo et ses collègues de l'UCLA. Crédit : Shreya Udani/UCLA
Aujourd’hui, les médicaments à base d’anticorps – des protéines qui combattent les infections et les maladies – sont prescrits pour tout, du cancer au COVID-19 en passant par l’hypercholestérolémie. Les anticorps sont fournis par des cellules génétiquement modifiées qui fonctionnent comme de minuscules usines de production de protéines en laboratoire.
Pendant ce temps, les chercheurs ciblent le cancer, les lésions des organes internes et une foule d’autres maladies avec de nouvelles stratégies dans lesquelles des cellules conçues de manière similaire sont implantées directement dans les patients.
Ces applications biotechnologiques reposent sur le principe selon lequel la modification de l'ADN d'une cellule afin de produire davantage d'instructions génétiques nécessaires à la fabrication d'une protéine donnée entraînera la libération par la cellule d'une plus grande quantité de cette protéine.
Une nouvelle étude de l'UCLA suggère que, au moins dans un type de cellules souches, ce principe n'est pas nécessairement vrai.
Les chercheurs ont examiné les cellules souches mésenchymateuses, qui résident dans la moelle osseuse et peuvent s'auto-renouveler ou se développer en cellules osseuses, adipeuses ou musculaires. Les cellules mésenchymateuses sécrètent un facteur de croissance protéique appelé VEGF-A, qui joue un rôle dans la régénération des vaisseaux sanguins et qui, selon les scientifiques, pourrait avoir le potentiel de réparer les dommages causés par les crises cardiaques, les lésions rénales, les maladies artérielles des membres et d'autres affections.
Lorsque les chercheurs ont comparé la quantité de VEGF-A libérée par chaque cellule mésenchymateuse avec l’expression de gènes dans la même cellule codant pour le VEGF-A, les résultats ont été surprenants : l’expression des gènes n’était que faiblement corrélée à la sécrétion réelle du facteur de croissance.
Les scientifiques ont identifié d'autres gènes mieux corrélés à la sécrétion de facteurs de croissance, dont un qui code pour une protéine présente à la surface de certaines cellules souches. En isolant les cellules souches avec cette protéine à leur surface, l’équipe a cultivé une population qui sécrétait de manière prolifique le VEGF-A et a continué à le faire quelques jours plus tard.
Les résultats, publiés dans Nature Nanotechnologiesuggèrent qu'une hypothèse fondamentale en biologie et en biotechnologie pourrait être reconsidérée, a déclaré l'auteur co-correspondant Dino Di Carlo, professeur d'ingénierie et de médecine Armond et Elena Hairapetian à l'école d'ingénierie UCLA Samueli.
“Le dogme central est le suivant: vous avez des instructions dans l'ADN, elles sont transcrites en ARN, puis l'ARN est traduit en protéine”, a déclaré Di Carlo, qui est également membre du California NanoSystems Institute de l'UCLA et d'Eli et Edythe Broad. Centre de médecine régénérative et de recherche sur les cellules souches.
“Sur cette base, de nombreux scientifiques ont supposé que si vous aviez plus d'ARN, vous auriez plus de protéines, puis plus de protéines libérées par la cellule. Nous avons remis en question cette hypothèse.
“Il semble que nous ne pouvons pas supposer que si un gène est exprimé à des niveaux plus élevés, il y aura une sécrétion plus élevée de la protéine correspondante. Nous avons trouvé un exemple clair où cela ne se produit pas, et cela ouvre de nombreuses nouvelles questions. “
Les résultats pourraient contribuer à rendre la fabrication de traitements à base d’anticorps plus efficace et à définir de nouveaux traitements cellulaires plus efficaces. Connaître les bons commutateurs génétiques à inverser pourrait permettre l’ingénierie ou la sélection de cellules extraordinairement productives pour la fabrication ou l’administration de thérapies.
L'étude de l'UCLA a été menée à l'aide d'un équipement de laboratoire standard complété par une technologie inventée par Di Carlo et ses collègues : des nanovials, des récipients microscopiques d'hydrogel en forme de bol, dont chacun capture une seule cellule et ses sécrétions.
En tirant parti d'une nouvelle méthode analytique basée sur les nanovioles, les scientifiques ont pu relier la quantité de VEGF-A libérée par chacune des 10 000 cellules souches mésenchymateuses à un atlas cartographiant des dizaines de milliers de gènes exprimés par cette même cellule.
“La capacité de lier la sécrétion de protéines à l'expression des gènes au niveau cellulaire est très prometteuse pour les domaines de la recherche en sciences de la vie et du développement thérapeutique”, a déclaré Kathrin Plath, professeur de chimie biologique à l'UCLA, membre du Broad Stem Cell Research. Center et auteur co-correspondant de l’étude.
“Sans cela, nous n'aurions pas pu arriver aux résultats inattendus que nous avons trouvés dans cette étude. Nous avons maintenant une opportunité passionnante d'apprendre de nouvelles choses sur les mécanismes qui sous-tendent les processus fondamentaux de la vie et d'utiliser ce que nous avons appris pour faire progresser la santé humaine.”
Alors que l'activation des instructions génétiques pour le VEGF-A présentait peu de corrélation avec la libération de la protéine, les chercheurs ont identifié un groupe de 153 gènes ayant des liens étroits avec la sécrétion du VEGF-A. Beaucoup d’entre eux sont connus pour leur fonction dans le développement des vaisseaux sanguins et la cicatrisation des plaies ; pour d’autres, leur fonction est actuellement inconnue.
L’une des principales correspondances code pour une protéine de surface cellulaire, IL13RA2, dont le but est mal compris. Son emplacement extérieur a permis aux scientifiques de l’utiliser plus facilement comme marqueur et de séparer ces cellules des autres. Les cellules avec IL13RA2 présentaient une sécrétion de VEGF-A 30 % plus élevée que les cellules dépourvues du marqueur.
Dans une expérience similaire, les chercheurs ont maintenu les cellules séparées en culture pendant six jours. À la fin de cette période, les cellules portant le marqueur sécrétaient 60 % plus de VEGF-A que les cellules sans ce marqueur.
Bien que les thérapies basées sur les cellules souches mésenchymateuses se soient révélées prometteuses dans des études en laboratoire, des essais cliniques menés auprès de participants humains ont montré que bon nombre de ces nouvelles options étaient sûres mais inefficaces. La capacité de trier les sécréteurs élevés de VEGF-A à l’aide d’IL13RA2 pourrait aider à inverser cette tendance.
“Identifier une sous-population qui produit davantage et les marqueurs associés à cette population signifie que vous pouvez les séparer très facilement”, a déclaré Di Carlo. “Une population de cellules très pures qui va produire des niveaux élevés de votre protéine thérapeutique devrait constituer une meilleure thérapie.”
Les nanovials sont disponibles dans le commerce auprès de Partillion Bioscience, une société cofondée par Di Carlo qui a démarré dans l'incubateur sur le campus du CNSI, Magnify.
Plus d'information:
Shreya Udani et al, Associant les sécrétions de facteurs de croissance et les transcriptomes de cellules uniques dans des nanovials à l'aide de SEC-seq, Nature Nanotechnologie (2023). DOI : 10.1038/s41565-023-01560-7
Fourni par l'Université de Californie, Los Angeles
Citation: Le « dogme central » de la biologie pourrait-il induire en erreur les bio-ingénieurs ? (12 décembre 2023) récupéré le 12 décembre 2023 sur
Ce document est soumis au droit d'auteur. En dehors de toute utilisation équitable à des fins d'étude ou de recherche privée, aucune partie ne peut être reproduite sans autorisation écrite. Le contenu est fourni seulement pour information.
