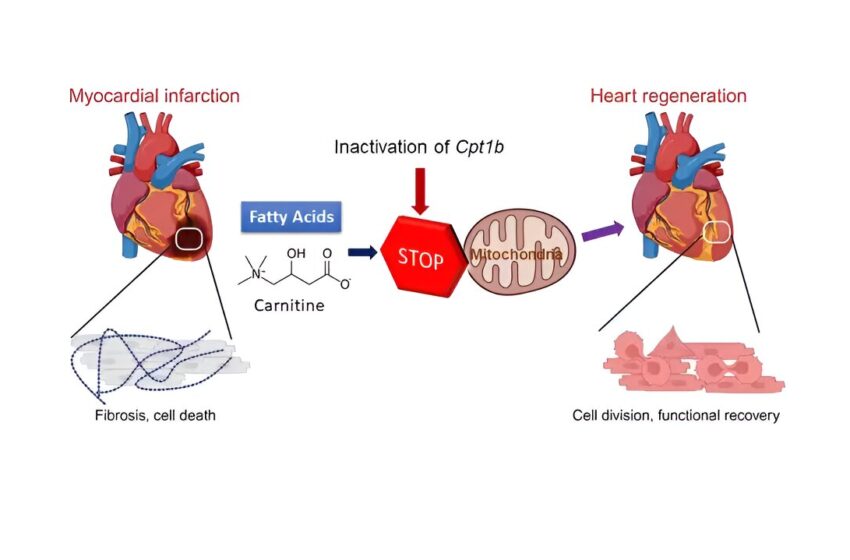
La reprogrammation du métabolisme énergétique rétablit la fonction cardiaque après un infarctus chez la souris
Chez les souris possédant un gène Cpt1b inactif, le cœur peut se régénérer après un infarctus. Crédit : MPI pour la recherche sur le cœur et les poumons, créé avec Biorender.com
Après la naissance, le cœur humain perd presque complètement sa capacité de régénération. Les dommages au muscle cardiaque, dus par exemple à une crise cardiaque, entraînent donc généralement une perte permanente de fonction chez l’adulte. Des scientifiques de l’Institut Max Planck de recherche sur le cœur et les poumons ont montré pour la première fois chez la souris qu’une modification du métabolisme énergétique des cellules du muscle cardiaque permet la régénération du cœur.
Chez les animaux, la fonction cardiaque pourrait ainsi être restaurée dans une large mesure après une crise cardiaque. L’étude, publiée dans la revue Natureest révolutionnaire et pourrait permettre des approches thérapeutiques complètement nouvelles.
La perte de capacité de régénération du cœur des adultes est due, entre autres, à la perte de la capacité des cellules du muscle cardiaque à se diviser après la naissance. Cela s’accompagne d’un changement fondamental dans le métabolisme énergétique des cellules cardiaques : au lieu de tirer leur énergie des sucres, ce que l’on appelle la glycolyse, les cellules du muscle cardiaque tirent désormais leur énergie en grande partie des graisses. Cette forme de production d’énergie est connue sous le nom d’oxydation des acides gras.
Le groupe de recherche dirigé par Thomas Braun, directeur de l’Institut Max Planck de recherche sur le cœur et les poumons à Bad Nauheim, en Allemagne, a commencé à rechercher de nouvelles méthodes pour favoriser la régénération cardiaque. “On sait que les espèces animales capables de régénérer leur cœur utilisent principalement les sucres et la glycolyse comme carburant pour les cellules du muscle cardiaque. Le cœur humain utilise également principalement la glycolyse aux premiers stades de son développement, mais passe ensuite à l’oxydation des acides gras car il peut produire plus d’énergie. “, expliquent Xiang Li et Xuejun Yuan, auteurs de l’étude.
“Avec le changement de production d’énergie après la naissance, l’activité de nombreux gènes change et l’activité de division cellulaire est perdue. Les métabolites individuels issus de la production d’énergie ont également des fonctions importantes pour l’activité des enzymes qui régulent l’activité des gènes. Nous espérions donc déclencher des changements dans la production d’énergie. activités en reprogrammant le métabolisme énergétique pour réactiver la capacité de division cellulaire dans les cellules du muscle cardiaque.
Gène inactivé pour l’oxydation des acides gras
Pour ce faire, les chercheurs de Max Planck ont d’abord inactivé chez la souris un gène appelé Cpt1b, essentiel à l’oxydation des acides gras. “Nous avons ensuite observé que le cœur de ces souris recommençait à croître”, explique Li. Au cours de l’expérience, le nombre de cellules dans le cœur de ces souris a presque doublé. Dans l’étape suivante, les chercheurs de Bad Nauheim ont déclenché des crises cardiaques chez des souris chez lesquelles Cpt1b était désactivé.
Dans l’approche choisie, une phase de manque de flux sanguin vers le cœur est suivie d’une phase de reperfusion, au cours de laquelle le cœur est à nouveau rincé avec du sang oxygéné. “Ce modèle est comparable à un patient cardiaque dont le cœur est traité par l’insertion d’un stent en raison d’une occlusion des artères coronaires”, explique Yuan. L’effet a été impressionnant : autrement, les cicatrices courantes dans le muscle cardiaque étaient à peine visibles après des semaines et la contractilité des animaux sans Cpt1b est presque revenue aux niveaux d’avant l’infarctus.
Retrouver la capacité de se régénérer
Dans d’autres études, les scientifiques ont pu décrypter le mécanisme sous-jacent. “Dans les cellules du muscle cardiaque des souris avec le gène inactivé, nous avons trouvé un niveau d’alpha-cétoglutarate vingt fois plus élevé. Le niveau élevé de ce métabolite entraîne une augmentation significative de l’activité de l’enzyme KDM5”, explique Braun.
Cette enzyme est ce qu’on appelle l’histone déméthylase, qui élimine les groupes méthyle des histones et réduit ainsi l’activité de divers gènes. Le changement dans l’activité des gènes fait que les cellules du muscle cardiaque deviennent immatures et retrouvent ainsi la capacité de se régénérer.
Braun considère l’étude comme une véritable avancée. “En reprogrammant le métabolisme, nous doublons le nombre de cellules du muscle cardiaque et, après un infarctus, la fonction cardiaque est presque complètement restaurée.” De plus, il est en principe possible de bloquer pharmacologiquement l’activité de l’enzyme CPT1B, le produit génique de Cpt1b. Le développement d’un inhibiteur pouvant être utilisé pour affecter l’activité de l’enzyme CPT1B est la prochaine étape vers le développement d’une thérapie qui pourrait éventuellement être utilisée chez l’homme.
Cependant, Yuan et Braun soulignent : « Nous avons encore un long chemin à parcourir avant que des traitements fiables chez l’homme ne deviennent possibles. La mise en œuvre des nouveaux résultats de la recherche fondamentale est longue et coûteuse et s’accompagne souvent de nombreux problèmes inattendus. Néanmoins, nous sommes confiants. que nous pourrons stimuler thérapeutiquement la capacité régénératrice du cœur à l’avenir.
Plus d’information:
Xiang Li et al, L’inhibition de l’oxydation des acides gras permet la régénération cardiaque chez la souris adulte, Nature (2023). DOI : 10.1038/s41586-023-06585-5
Fourni par la Société Max Planck
Citation: La reprogrammation du métabolisme énergétique rétablit la fonction cardiaque après un infarctus chez la souris (24 octobre 2023) récupéré le 24 octobre 2023 sur
Ce document est soumis au droit d’auteur. En dehors de toute utilisation équitable à des fins d’étude ou de recherche privée, aucune partie ne peut être reproduite sans autorisation écrite. Le contenu est fourni seulement pour information.
