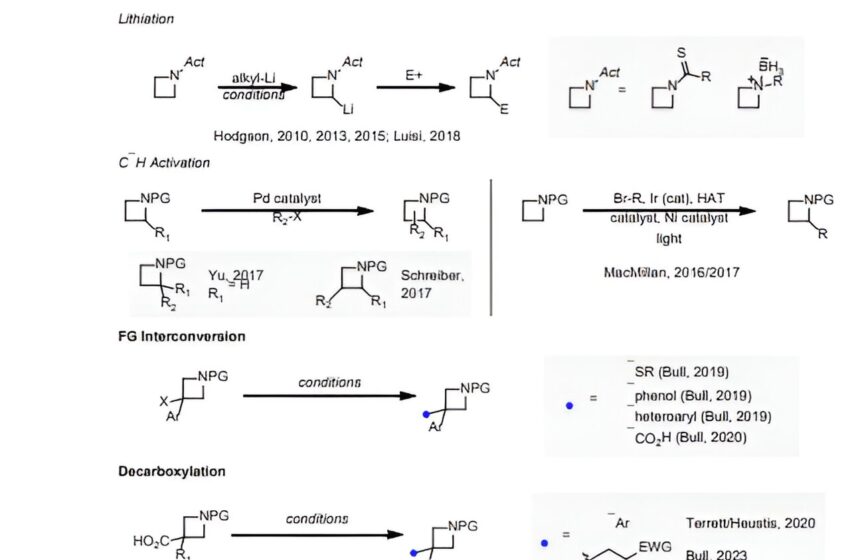
Les scientifiques utilisent la modélisation informatique pour guider une synthèse chimique difficile
Crédit: Science (2024). DOI : 10.1126/science.adj6771
Des chercheurs du MIT et de l’Université du Michigan ont découvert une nouvelle façon de déclencher des réactions chimiques susceptibles de générer une grande variété de composés dotés de propriétés pharmaceutiques souhaitables.
Ces composés, appelés azétidines, sont caractérisés par des cycles à quatre chaînons contenant de l’azote. Les azétidines ont traditionnellement été beaucoup plus difficiles à synthétiser que les cycles à cinq chaînons contenant de l’azote, que l’on trouve dans de nombreux médicaments approuvés par la FDA.
La réaction utilisée par les chercheurs pour créer des azétidines est provoquée par un photocatalyseur qui excite les molécules à partir de leur état d’énergie fondamentale. À l’aide de modèles informatiques qu’ils ont développés, les chercheurs ont pu prédire les composés qui peuvent réagir entre eux pour former des azétidines en utilisant ce type de catalyse.
“À l’avenir, plutôt que de recourir à un processus d’essais et d’erreurs, les gens pourront présélectionner les composés et savoir à l’avance quels substrats fonctionneront et lesquels ne fonctionneront pas”, explique Heather Kulik, professeure agrégée de chimie et de génie chimique au MIT.
Kulik et Corinna Schindler, professeur de chimie à l’Université du Michigan, sont les auteurs principaux de l’étude, qui paraît aujourd’hui dans ScienceEmily Wearing, récemment diplômée de l’Université du Michigan, est l’auteure principale de l’article. Parmi les autres auteurs figurent Yu-Cheng Yeh, postdoctorant de l’Université du Michigan, Gianmarco Terrones, étudiant diplômé du MIT, Seren Parikh, étudiante diplômée de l’Université du Michigan, et Ilia Kevlishvili, postdoctorant du MIT.
Synthèse pilotée par la lumière
De nombreuses molécules naturelles, dont les vitamines, les acides nucléiques, les enzymes et les hormones, contiennent des cycles azotés à cinq chaînons, également appelés hétérocycles azotés. Ces cycles se retrouvent également dans plus de la moitié de tous les médicaments à petites molécules approuvés par la FDA, dont de nombreux antibiotiques et médicaments contre le cancer.
Les hétérocycles azotés à quatre chaînons, que l’on trouve rarement dans la nature, présentent également un potentiel en tant que composés médicamenteux. Cependant, seule une poignée de médicaments existants, y compris la pénicilline, contiennent des hétérocycles à quatre chaînons, en partie parce que ces cycles à quatre chaînons sont beaucoup plus difficiles à synthétiser que les hétérocycles à cinq chaînons.
Ces dernières années, le laboratoire de Schindler a travaillé sur la synthèse d’azétidines en utilisant la lumière pour déclencher une réaction qui combine deux précurseurs, un alcène et une oxime. Ces réactions nécessitent un photocatalyseur, qui absorbe la lumière et transmet l’énergie aux réactifs, leur permettant ainsi de réagir entre eux.
“Le catalyseur peut transférer cette énergie à une autre molécule, ce qui déplace les molécules dans des états excités et les rend plus réactives. C’est un outil que les gens commencent à utiliser pour permettre de provoquer certaines réactions qui ne se produiraient normalement pas”, ” dit Kulik.
Le laboratoire de Schindler a découvert que si cette réaction fonctionnait parfois bien, d’autres fois non, selon les réactifs utilisés. Ils ont fait appel à Kulik, un expert dans le développement d’approches informatiques pour modéliser les réactions chimiques, pour les aider à comprendre comment prédire quand ces réactions se produiront.
Les deux laboratoires ont émis l’hypothèse que la réaction d’un alcène et d’une oxime particuliers dans une réaction photocatalysée dépend d’une propriété connue sous le nom de correspondance d’énergie orbitale frontière. Les électrons qui entourent le noyau d’un atome existent dans des orbitales et la mécanique quantique peut être utilisée pour prédire la forme et les énergies de ces orbitales. Pour les réactions chimiques, les électrons les plus importants sont ceux qui se trouvent dans les orbitales les plus externes et les plus énergétiques (« frontières »), qui sont disponibles pour réagir avec d’autres molécules.
Kulik et ses étudiants ont utilisé la théorie de la fonctionnelle de la densité, qui utilise l’équation de Schrödinger pour prédire où les électrons pourraient se trouver et quelle quantité d’énergie ils ont, pour calculer l’énergie orbitale de ces électrons les plus externes.
Ces niveaux d’énergie sont également affectés par d’autres groupes d’atomes attachés à la molécule, ce qui peut modifier les propriétés des électrons dans les orbitales les plus externes.
Une fois ces niveaux d’énergie calculés, les chercheurs peuvent identifier les réactifs qui ont des niveaux d’énergie similaires lorsque le photocatalyseur les propulse dans un état excité. Lorsque les états excités d’un alcène et d’une oxime sont étroitement identiques, moins d’énergie est nécessaire pour propulser la réaction vers son état de transition, le point auquel la réaction a suffisamment d’énergie pour progresser et former des produits.
Des prévisions précises
Après avoir calculé les énergies orbitales de frontière pour 16 alcènes et neuf oximes différents, les chercheurs ont utilisé leur modèle informatique pour prédire si 18 paires alcène-oxime différentes réagiraient ensemble pour former une azétidine. Grâce aux calculs en main, ces prédictions peuvent être faites en quelques secondes.
Les chercheurs ont également modélisé un facteur qui influence le rendement global de la réaction : une mesure de la disponibilité des atomes de carbone dans l’oxime pour participer aux réactions chimiques.
Les prédictions du modèle suggèrent que certaines de ces 18 réactions ne se produiront pas ou ne donneront pas un rendement suffisamment élevé. Cependant, l’étude a également montré qu’un nombre important de réactions sont correctement prédites qu’elles fonctionneront.
« D’après notre modèle, il existe une gamme de substrats pour cette synthèse d’azétidine bien plus large que ce que l’on pensait auparavant. Les gens ne pensaient pas vraiment que tout cela était accessible », explique Kulik.
Sur les 27 combinaisons étudiées par ordinateur, les chercheurs ont testé expérimentalement 18 réactions et ont constaté que la plupart de leurs prédictions étaient exactes. Parmi les composés synthétisés se trouvaient des dérivés de deux composés médicamenteux actuellement approuvés par la FDA : l’amoxapine, un antidépresseur, et l’indométacine, un analgésique utilisé pour traiter l’arthrite.
Cette approche informatique pourrait aider les sociétés pharmaceutiques à prédire les molécules qui réagiront ensemble pour former des composés potentiellement utiles, avant de dépenser beaucoup d’argent pour développer une synthèse qui pourrait ne pas fonctionner, explique Kulik. Elle et Schindler continuent de travailler ensemble sur d’autres types de synthèses nouvelles, notamment la formation de composés comportant des cycles à trois chaînons.
“L’utilisation de photocatalyseurs pour exciter des substrats est un domaine de développement très actif et brûlant, car les gens ont épuisé ce que l’on pouvait faire avec l’état fondamental ou avec la chimie radicale”, explique Kulik. “Je pense que cette approche aura beaucoup plus d’applications pour fabriquer des molécules qui sont normalement considérées comme très difficiles à fabriquer.”
Plus d’information:
Emily R. Wearing et al., Réaction de Paternò-Büchi médiée par la lumière visible des oximes acycliques et des alcènes en azétidines, Science (2024). DOI : 10.1126/science.adj6771
Fourni par le Massachusetts Institute of Technology
Citation: Les scientifiques utilisent la modélisation informatique pour guider une synthèse chimique difficile (27 juin 2024) récupéré le 27 juin 2024 sur
Ce document est soumis au droit d’auteur. En dehors de toute utilisation équitable à des fins d’étude ou de recherche privée, aucune partie ne peut être reproduite sans autorisation écrite. Le contenu est fourni à titre d’information uniquement.
