Une étude explique pourquoi de nombreux médicaments contre le cancer échouent lors des essais cliniques
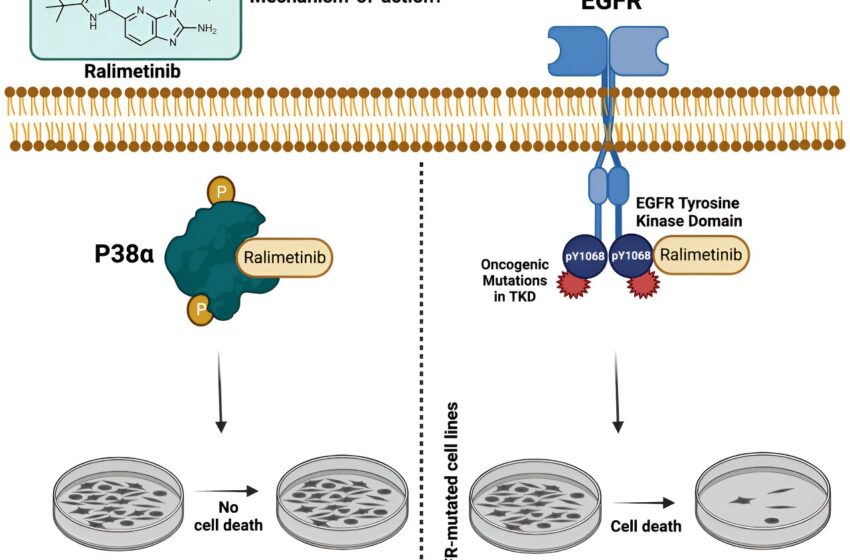
Résumé graphique. Crédit: Biologie chimique cellulaire (2023). DOI : 10.1016/j.chambiol.2023.09.013
Souvent, les médicaments contre le cancer ne se comportent pas comme prévu lors des essais cliniques. Une étude publiée le 11 octobre dans la revue Biologie chimique cellulaire explore pourquoi il est peu probable que les médicaments en cours de développement fonctionnent en raison d’une analyse génétique insuffisante.
Les médicaments anticancéreux, conçus pour cibler une seule protéine mutée et ne pas avoir d’impact sur les tissus normaux, échouent pour deux raisons. “Ils sont trop toxiques pour que les patients puissent les prendre en toute sécurité, ou les patients peuvent les prendre en toute sécurité, mais ils ne réduisent pas réellement la tumeur d’un patient”, a déclaré l’auteur principal de l’étude, Jason Sheltzer, Ph.D., professeur adjoint de chirurgie et de génétique. et membre du Yale Cancer Center. Découvrir les mécanismes derrière un médicament mal caractérisé pourrait faire la lumière sur ses mauvaises performances dans les essais cliniques.
La plupart des médicaments anticancéreux ne parviennent pas à recevoir l’approbation de la Food and Drug Administration des États-Unis. Pour comprendre pourquoi, Debanjan Bhattacharjee, Ph.D., et Jaweria Bakar du Sheltzer Lab ont étudié un médicament inhibiteur de p38a appelé ralimetinib.
“Lorsque nous avons testé ce médicament dans notre laboratoire, nous avons constaté qu’il ciblait une voie différente”, a déclaré Sheltzer. Aucun des patients n’a répondu puisque la sensibilité cellulaire au ralimetinib présentait la plus forte corrélation avec les inhibiteurs de l’EGFR. “Si vous comparez les types de cancer pour lesquels ce médicament a été testé par rapport aux types de cancer connus pour être provoqués par l’EGFR, il n’y a tout simplement pas de chevauchement”, a déclaré Sheltzer.
“Souvent, les chercheurs développent un médicament et constatent que le médicament tue les cellules cancéreuses. Et cela suffira à motiver un essai. Mais il n’y a aucune compréhension génétique de la façon dont il tue les cellules cancéreuses ou pourquoi il tue les cellules cancéreuses. Et sans cela. compréhension génétique, vous ne savez pas réellement à quels patients atteints de cancer le donner, car vous ne savez pas quels biomarqueurs ou altérations génétiques rechercher dans la tumeur d’un patient afin de lui administrer ce médicament”, a déclaré Sheltzer.
Les scientifiques ont besoin d’une approche multimodale pour cibler les mécanismes sous-jacents de la maladie. “Si nous avions eu cette compréhension génétique du médicament plus tôt, il aurait pu être administré à un groupe différent de patients qui auraient été plus susceptibles de répondre”, a déclaré Sheltzer. Les scientifiques peuvent rassembler des preuves à l’aide d’une combinaison d’outils, notamment CRISPR, le profilage pharmacogénomique et l’évaluation structurelle.
Bien que des tests supplémentaires soient nécessaires, une approche axée sur la génétique a de vastes applications dans la lutte contre le cancer. L’analyse génétique dans un environnement multidisciplinaire est fondamentale pour améliorer le taux de réussite des nouvelles thérapies.
Plus d’information:
Debanjan Bhattacharjee et al, L’inhibition d’une cible de puissance inférieure entraîne l’activité anticancéreuse d’un inhibiteur clinique de p38, Biologie chimique cellulaire (2023). DOI : 10.1016/j.chambiol.2023.09.013
Fourni par l’Université de Yale
Citation: Une étude explique pourquoi de nombreux médicaments anticancéreux échouent lors des essais cliniques (25 octobre 2023) récupéré le 25 octobre 2023 sur
Ce document est soumis au droit d’auteur. En dehors de toute utilisation équitable à des fins d’étude ou de recherche privée, aucune partie ne peut être reproduite sans autorisation écrite. Le contenu est fourni seulement pour information.
