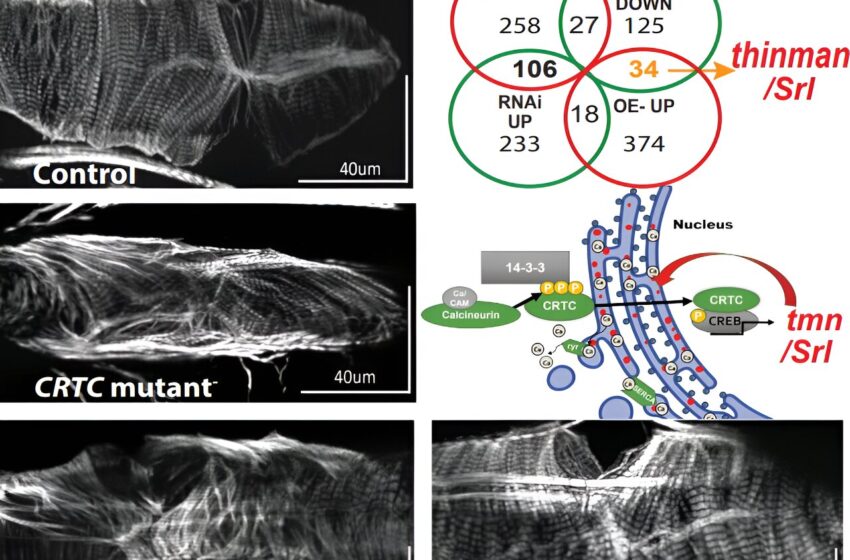
Le contrôle de l’épaisseur des cœurs de mouches à fruits révèle une nouvelle voie de développement des maladies cardiaques
Ce résumé graphique utilise des images des expériences de l’étude pour mettre en évidence les principales découvertes concernant le rôle d’une protéine appelée coactivateur de transcription régulé par CREB (CRTC) dans le soutien du maintien de la structure et de la fonction cardiaque, et comment elle est probablement l’une des sources sous-jacentes de l’hypertrophie cardiaque. Crédit : Karen Ocorr
Des scientifiques de Sanford Burnham Prebys et du Salk Institute for Biological Studies ont découvert un nouveau rôle pour une protéine connue pour son rôle dans le cerveau, qui aide à contrôler les sensations de faim ou de satiété, ainsi que dans le foie, pour aider le corps à maintenir un équilibre énergétique pendant le jeûne. La nouvelle étude montre que cette protéine contribue également au maintien de la structure et de la fonction cardiaque, mais lorsqu’elle est hyperactive, elle provoque un épaississement du muscle cardiaque, associé aux maladies cardiaques.
L’épaississement excessif du muscle cardiaque, appelé hypertrophie cardiaque, est souvent le résultat de la tentative du cœur de maintenir un flux sanguin adéquat tout en s’adaptant aux changements causés par d’autres maladies cardiaques telles que l’hypertension ou le dysfonctionnement des valves cardiaques. L’hypertrophie du ventricule gauche du cœur touche jusqu’à la moitié de tous les patients diagnostiqués avec un diabète de type 2, et l’épaississement de cette cavité est connu pour entraîner davantage d’événements cardiovasculaires indésirables tels que des crises cardiaques, des accidents vasculaires cérébraux et des morts cardiaques subites.
« Nous nous intéressons à ce sujet car les maladies cardiaques sont la principale cause de décès dans le monde industrialisé », explique Karen Ocorr, Ph. D., professeure adjointe au sein du programme Développement, vieillissement et régénération à Sanford Burnham Prebys. « Et pour la plupart des cas, y compris l’hypertrophie cardiaque, nous ne connaissons toujours pas vraiment les causes profondes. »
Ocorr, son laboratoire et ses collaborateurs de l’Institut Salk ont publié les résultats le 1er août 2024, dans Rapports de cellulesmontrant qu’une protéine appelée coactivateur de transcription régulé par CREB (CRTC) est probablement l’une des sources sous-jacentes de l’hypertrophie cardiaque.
« On a beaucoup travaillé pour comprendre comment le CRTC fonctionne dans les neurones et le foie, mais personne n’a vraiment démontré qu’il fonctionne dans le cœur », explique Cristiana Dondi, Ph. D., associée postdoctorale au laboratoire Ocorr et première auteure de l’étude. « Nous étions déterminés à changer cela. »
L’équipe de recherche savait que le CRTC interagissait avec une enzyme appelée calcineurine, qui avait été associée à l’hypertrophie cardiaque lors d’études antérieures. Ils ont commencé par créer des mouches à fruits génétiquement modifiées avec une forme inactive du gène qui porte le schéma directeur du CRTC.
Lors de tests du rythme cardiaque à l’aide de minuscules électrodes et de la fonction cardiaque à l’aide d’images vidéo à haute vitesse, les mouches à fruits sans CRTC actif ont eu plus de difficultés à retrouver un rythme cardiaque normal après avoir subi un stress que les mouches à fruits normales. Les mouches modifiées avaient également des muscles cardiaques plus fins avec une fonction diminuée et étaient incapables de faire circuler le sang aussi efficacement.
« En plus des défauts structurels que nous avons trouvés chez les mouches dont le gène CRTC était systémiquement inactivé, nous avons également observé une quantité incroyable de fibrose », note Ocorr, auteur principal de l’étude. « Nous ne voyons pratiquement jamais cela dans les cœurs normaux, ce qui m’a vraiment frappé car la fibrose est une caractéristique des maladies cardiaques. »
Pour s’assurer que ces observations étaient spécifiquement liées à un manque de CRTC dans le cœur plutôt qu’à un défaut de développement plus large dans d’autres cellules qui précipitait le phénomène, l’équipe a étudié des mouches qui n’ont pas réussi à produire la protéine CRTC dans le cœur tandis que d’autres tissus ont maintenu leur production de CRTC.
« Nous avons obtenu des résultats très similaires à ceux des études réalisées avec nos mouches knock-out sur tout le corps, ce qui nous a permis de confirmer que les changements étaient spécifiques à un manque de CRTC dans le cœur », explique Dondi. Pour être encore plus sûr, le groupe a répété les expériences en éliminant le CRTC uniquement dans les cellules entourant le cœur, appelées cellules péricardiques, puis dans le système nerveux et, enfin, dans le corps adipeux de la mouche considéré comme l’équivalent du foie de la mouche. Mais aucune de ces manipulations n’a eu les mêmes effets sur le cœur, ce qui ajoute encore plus de poids au rôle cardiaque crucial du CRTC.
En plus d’examiner les effets d’une absence de CRTC dans le cœur, l’équipe a également étudié ce qui se passerait si le cœur produisait trop de CRTC, ce que l’on appelle une surexpression.
« Il semble que ce soit les deux faces d’une même pièce », ajoute Ocorr. « Sans CRTC, les fibres musculaires des cellules cardiaques se désorganisent. Elles commencent à avoir de grands espaces entre elles et la capacité du cœur à se contracter est alors réduite. »
« Si vous surexprimez le CRTC, vous obtenez l’effet inverse. Vous obtenez beaucoup plus de protéines que ce dont le cœur a normalement besoin, ce qui le fait grossir et provoque une hypertrophie. Bien que le cœur soit plus gros, il devient trop musclé et ne fonctionne pas aussi bien qu’un cœur normal. »
En plus de trouver un nouvel agent responsable de l’hypertrophie cardiaque aux côtés de l’enzyme calcineurine bien établie, Dondi, Ocorr et leurs collaborateurs ont découvert une protéine dont la production est contrôlée par le CRTC et contribue probablement aux malformations cardiaques observées dans cette publication.
« Nous avons vérifié comment les gènes fonctionnaient différemment dans les cœurs présentant une activité CRTC trop faible ou trop importante », explique Dondi. « Après avoir filtré les gènes présents dans les cellules cardiaques, nous avons réduit la liste à 15 gènes. »
L’un de ces 15 gènes est l’équivalent du gène humain chez la mouche à fruits Sarcaluménine qui s’est avéré plus actif lorsque le CRTC était surexprimé et moins actif lorsque le CRTC était silencieux. Lorsque les chercheurs ont empêché la production de cette protéine, ils ont observé des effets similaires sur la structure et la fonction cardiaques comme dans les expériences précédentes centrées sur le CRTC. Comme la perte de cette protéine a provoqué un amincissement du cœur, l’équipe a proposé de nommer ce gène «homme mince.“
« C’était une autre preuve que le CRTC contrôle la production de »homme mince” chez les mouches, et probablement aussi Sarcaluménine chez l’homme, lors d’un entretien cardiaque normal”, explique Ocorr. “Le homme mince Le gène contient des instructions pour les protéines impliquées dans la gestion des niveaux de calcium dans les cellules musculaires squelettiques et cardiaques. Si quelque chose arrive au CRTC, vous perdez Sarcaluménine ou homme mince et vous obtenez une surcharge en calcium et une désorganisation musculaire. Nos études montrent que le CRTC-homme mince La connexion est une nouvelle voie dans l’hypertrophie cardiaque, ce qui constitue une nouvelle découverte très intéressante dans le domaine de la recherche cardiaque.
« Cette découverte ouvre de nombreuses possibilités pour en apprendre davantage sur ces molécules de signalisation et les utiliser comme cibles pour des médicaments destinés à traiter les maladies cardiaques. Sarcaluménine « Elle a également été associée à la dystrophie musculaire. Nous voyons donc de nombreuses possibilités d’élargir ces travaux pour trouver des traitements potentiels pour d’autres pathologies en plus des maladies cardiaques. »
Plus d’information:
Cristiana Dondi et al, Le capteur de nutriments CRTC et la sarcalumenine/thinman représentent une voie alternative dans l’hypertrophie cardiaque, Rapports de cellules (2024). DOI: 10.1016/j.celrep.2024.114549
Fourni par Sanford-Burnham Prebys
Citation: Le contrôle de l’épaisseur des cœurs de mouches à fruits révèle une nouvelle voie pour les maladies cardiaques (2024, 2 août) récupéré le 2 août 2024 à partir de
Ce document est soumis au droit d’auteur. En dehors de toute utilisation équitable à des fins d’étude ou de recherche privée, aucune partie ne peut être reproduite sans autorisation écrite. Le contenu est fourni à titre d’information uniquement.
