Des scientifiques découvrent une cible antidépressive à action rapide et à faibles effets secondaires
Des chercheurs de l’Université des sciences de Tokyo découvrent les mécanismes cellulaires et moléculaires qui sous-tendent les effets de type antidépresseur des agonistes des récepteurs opioïdes delta, ouvrant la voie à son développement clinique en tant que thérapeutique à action rapide avec des effets secondaires minimes par rapport aux antidépresseurs conventionnels. Crédit : Prof. Akiyoshi Saitoh, TUS, Japon sur www.nature.com/articles/s41380-024-02814-z#citeas
Le fardeau mondial des troubles liés à l’anxiété et à la dépression est en augmentation. Bien que plusieurs médicaments aient été développés pour traiter ces affections, les médicaments actuels présentent plusieurs limites, notamment une action lente et des effets indésirables en cas d’utilisation à long terme. Cela souligne le besoin urgent de nouveaux agents thérapeutiques à action rapide et avec un minimum d’effets secondaires.
Le récepteur opioïde delta (DOP) joue un rôle clé dans la régulation de l’humeur, ce qui en fait une cible prometteuse pour une intervention thérapeutique. Des études ont montré que les agonistes sélectifs de la DOP (composés qui activent la DOP), tels que SNC80 et KNT-127, exercent des effets antidépresseurs et anxiolytiques (anti-anxiété) dans des modèles animaux.
Cependant, les mécanismes moléculaires précis qui sous-tendent leurs actions restent flous. Comprendre les mécanismes neurologiques qui sous-tendent la régulation de l’humeur et l’action de la DOP est crucial pour faire progresser les agonistes de la DOP en tant qu’agents thérapeutiques.
À cette fin, le professeur Akiyoshi Saitoh et M. Toshinori Yoshioka de l’Université des sciences de Tokyo (TUS), au Japon, ont mené une série d’expériences pour élucider les processus cellulaires et moléculaires contribuant aux effets antidépresseurs du KNT-127.
Apporter un aperçu plus approfondi de leurs travaux publiés en ligne le 6 décembre 2024 dans Psychiatrie Moléculairedéclare le professeur Saitoh : « En combinant les résultats de cette étude avec nos découvertes précédentes, nous pensons que les agonistes de la DOP ont un mécanisme d’action sans précédent et ont le potentiel de révolutionner le traitement de la dépression avec une efficacité et une sécurité supérieures à celles des médicaments existants.
Dans leurs travaux précédents, les chercheurs ont mené le test de nage forcée (FST), connu pour induire un comportement d’impuissance de type dépression chez des souris non testées, afin de déterminer si le KNT-127 produit des effets de type antidépresseur.
Ils ont comparé la réponse des animaux traités avec KNT-127 et des témoins. Notamment, une seule injection de KNT-127, 30 minutes avant le test, a considérablement réduit le nombre d’immobilités, reflétant un effet de type antidépresseur médié par la stimulation de la DOP.
La cible mécaniste (ou mammifère) de la voie de signalisation de la rapamycine (mTOR), impliquée dans les effets rapides des antidépresseurs, a été étudiée pour son rôle dans l’action du KNT-127. Les chercheurs ont injecté aux souris de la rapamycine, un inhibiteur de mTOR, avant le traitement par KNT-127.
En effet, la rapamycine a inversé la diminution du nombre d’immobilités FST induite par le KNT-127, indiquant que les effets de type antidépresseur du KNT-127 étaient médiés par la signalisation mTOR.
Ensuite, les chercheurs ont analysé l’activation des protéines liées à la signalisation mTOR dans les régions du cerveau associées aux troubles de l’humeur et ont cartographié des modèles de phosphorylation distincts dans le cortex préfrontal médial (mPFC), l’amygdale et l’hippocampe.
Les expériences ont révélé que les effets de type antidépresseur étaient principalement médiés par la signalisation Akt dans le mPFC, tandis que les effets anxiolytiques étaient associés à l’activation de l’amygdale via la signalisation ERK.
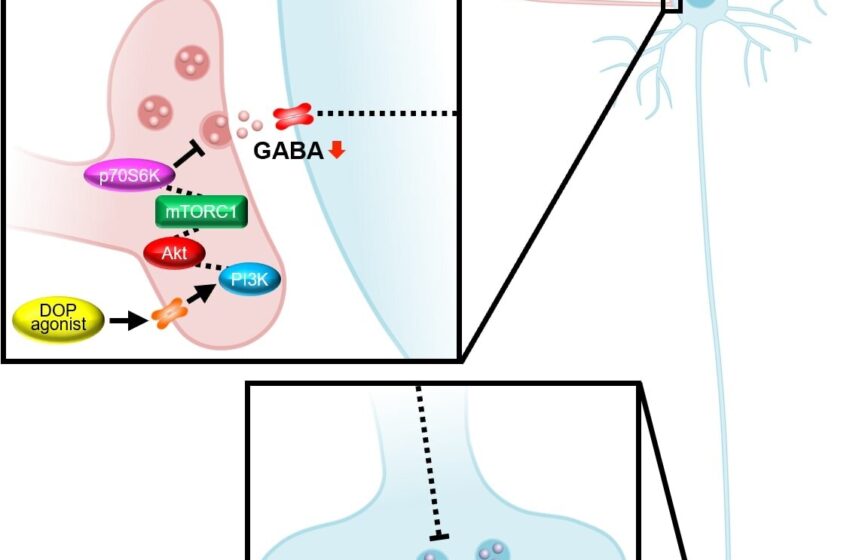
D’autres études sur un modèle murin de dépression ont révélé que lorsque KNT-127 était injecté localement dans la région médiale du cortex infralimbique préfrontal (IL-PFC), un effet antidépresseur était produit par les voies PI3K et mTOR. L’IL-PFC chez les rongeurs est considérée comme fonctionnellement similaire à la zone Brodmann 25 chez l’homme, qui est associée à la régulation de l’humeur.
De plus, les effets de type antidépresseur du KNT-127 étaient indépendants de la souche, du sexe ou de l’âge des animaux, et un autre agoniste de la DOP, le SNC80, présentait également des effets de type antidépresseur, soulignant le large potentiel thérapeutique des agonistes de la DOP.
De plus, l’application de KNT-127 au tissu cérébral isolé de l’IL-PFC a amélioré la transmission glutamatergique en supprimant la libération d’acide gamma-aminobutyrique (GABA, un neurotransmetteur clé), renforçant ainsi l’action directe des DOP sur l’IL-PFC.
L’étude a identifié que la plupart des DOP étaient exprimées dans les interneurones à parvalbumine positive dans l’IL-PFC, offrant ainsi de nouvelles informations sur l’expression spécifique des cellules de la DOP dans des régions distinctes du cerveau, élargissant ainsi notre compréhension de ses mécanismes.
Le professeur Saitoh conclut : « Nos résultats fournissent une preuve du mécanisme sous-jacent à l’effet antidépresseur de la DOP et peuvent considérablement stimuler le développement clinique d’agonistes de la DOP en tant que thérapeutiques. De plus, l’IL-PFC est la région impliquée dans la résistance au traitement par antidépresseurs conventionnels. Les agonistes du DOP pourraient donc être plus efficaces chez les patients qui présentent une résistance aux thérapies existantes. »
Plus d’informations :
Toshinori Yoshioka et al, les agonistes des récepteurs opioïdes Delta activent la signalisation PI3K – mTORC1 dans les interneurones à parvalbumine positive dans le cortex préfrontal infralimbique de souris pour exercer des effets aigus de mensonge antidépresseur, Psychiatrie Moléculaire (2024). DOI : 10.1038/s41380-024-02814-z
Fourni par l’Université des sciences de Tokyo
Citation: Des scientifiques découvrent une cible d’antidépresseurs à action rapide et à faibles effets secondaires (14 janvier 2025) récupéré le 14 janvier 2025 sur
Ce document est soumis au droit d’auteur. En dehors de toute utilisation équitable à des fins d’étude ou de recherche privée, aucune partie ne peut être reproduite sans autorisation écrite. Le contenu est fourni à titre informatif uniquement.
