Des simulations informatiques clarifient la propagation du cancer du sein
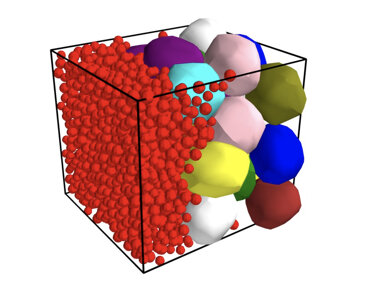
Simulation informatique de cellules cancéreuses et de tissu mammaire. Crédit : Université Yale
En utilisant une combinaison de simulations informatiques et d’études expérimentales, une équipe de chercheurs découvre des indices essentiels sur la manière dont les cellules cancéreuses du sein envahissent le tissu mammaire.
Dans les modèles de souris traditionnels utilisés pour étudier l’invasion du cancer du sein, les chercheurs prélèvent de fines tranches d’une tumeur induite chez une souris et les examinent au microscope. Cette procédure fournit des informations précieuses sur l’invasion du cancer du sein, a déclaré Corey O’Hern, auteur principal de l’étude, mais elle est limitée à de nombreux égards.
« Le problème des études actuelles sur les modèles murins est que les études histologiques ne donnent que de fines tranches d’une tumeur à un moment précis », a déclaré O’Hern, professeur de génie mécanique et de science des matériaux, de physique et de physique appliquée. « Elles ne permettent pas aux chercheurs de suivre l’évolution spatio-temporelle de l’invasion des cellules cancéreuses. »
À cette fin, l’équipe de recherche a développé un nouveau modèle informatique pour l’invasion du cancer du sein. « Grâce à ces nouveaux modèles informatiques, nous pouvons désormais déterminer comment les cellules cancéreuses envahissent le tissu mammaire en trois dimensions en fonction du temps. Par exemple, nous pouvons prédire à quelle vitesse les cellules cancéreuses doivent se déplacer sur une distance donnée à travers un tissu mammaire dense. »
En plus des modèles informatiques, l’équipe développe également des expériences in vitro : des systèmes modèles composés de billes de la taille d’un micron mélangées à des fibres de collagène qui reproduisent de nombreuses caractéristiques du cancer du sein dans des modèles animaux et permettent de valider les simulations informatiques.
O’Hern a dirigé les simulations informatiques, tandis que les expériences in vitro ont été menées par le professeur Claudia Fischbach de l’Université Cornell. L’étude a été publiée dans Bio-ingénierie APL.
Les chercheurs se sont particulièrement intéressés aux tumeurs mammaires qui naissent dans la paroi épithéliale des canaux galactophores. Les cellules épithéliales saines restent ensemble et forment la paroi des canaux galactophores. Mais lorsqu’elles deviennent cancéreuses, elles deviennent mobiles, se séparent les unes des autres et se déplacent hors des canaux galactophores vers le tissu adipeux environnant, composé de cellules adipeuses.
Le nombre de cellules cancéreuses qui progressent dans le tissu adipeux détermine la probabilité qu’elles envahissent les vaisseaux sanguins et forment des tumeurs secondaires.
« Nous souhaitons comprendre ce processus car lorsque les cellules cancéreuses envahissent le tissu adipeux, elles sont plus susceptibles de métastaser et de former des tumeurs secondaires qui sont rarement curables », a-t-il déclaré. « Si les cellules cancéreuses étaient localisées dans les canaux galactophores, le cancer du sein serait beaucoup plus facile à traiter. »
Outre la viscosité des cellules cancéreuses, les chercheurs étudient également d’autres variables, notamment la rigidité des cellules adipeuses, car les cellules moins déformables rendent plus difficile l’invasion du tissu adipeux par les cellules cancéreuses. Un autre facteur est la taille des espaces entre les cellules adipeuses et la mesure dans laquelle la matrice extracellulaire (ECM) à l’intérieur de ces espaces est alignée pour permettre une migration efficace des cellules cancéreuses.
« Les cellules cancéreuses se déplacent-elles de manière balistique ou diffuse ? Peuvent-elles se déplacer suffisamment vite pour déformer les adipocytes ? Si nous comprenons ces questions, nous pouvons comprendre le mécanisme physique par lequel les cellules cancéreuses se déplacent dans un tissu adipeux très dense. »
En l’absence de « minuscules caméras » capables d’observer l’invasion du cancer du sein en temps réel, a déclaré O’Hern, l’approche à deux volets de simulations informatiques et d’expériences in vitro pourrait être la meilleure approche.
Grâce à cette approche, a-t-il déclaré, ils ont pu prouver que l’activité et l’adhérence des cellules cancéreuses, la rigidité des cellules adipeuses et le confinement de la matrice extracellulaire contrôlent la transition entre la non-invasion et l’invasion des cellules cancéreuses dans le tissu adipeux.
Plus d’information:
Yitong Zheng et al, Modélisation informatique des caractéristiques physiques qui influencent l’invasion du cancer du sein dans le tissu adipeux, Bio-ingénierie APL (2024). DOI: 10.1063/5.0209019
Fourni par l’Université Yale
Citation: Des simulations informatiques clarifient la propagation du cancer du sein (2024, 8 août) récupéré le 8 août 2024 à partir de
Ce document est soumis au droit d’auteur. En dehors de toute utilisation équitable à des fins d’étude ou de recherche privée, aucune partie ne peut être reproduite sans autorisation écrite. Le contenu est fourni à titre d’information uniquement.
