Des chercheurs développent un modèle d’IA qui prédit la précision de la liaison protéine-ADN
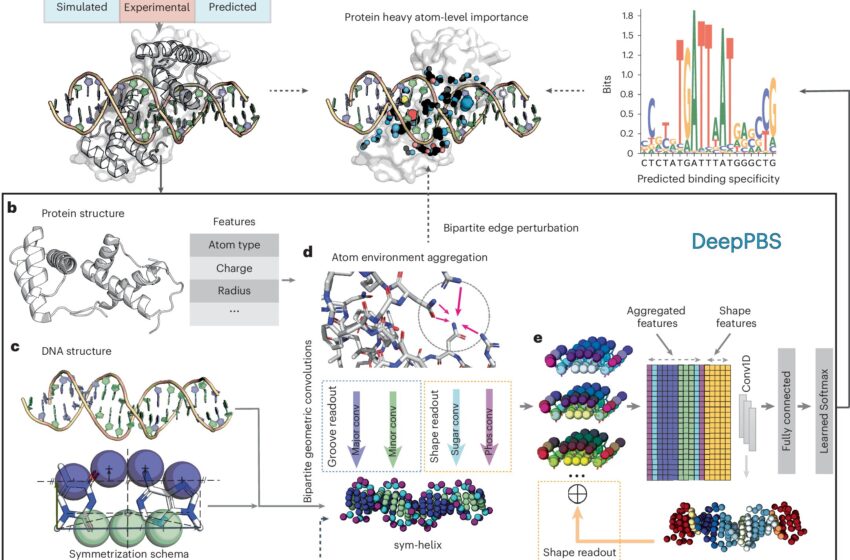
Illustration schématique du cadre DeepPBS. Crédit : Méthodes de la nature (2024). DOI: 10.1038/s41592-024-02372-w
Un nouveau modèle d’intelligence artificielle développé par des chercheurs de l’USC et publié dans Méthodes de la nature peut prédire avec précision comment différentes protéines peuvent se lier à l’ADN pour différents types de protéines, une avancée technologique qui promet de réduire le temps nécessaire au développement de nouveaux médicaments et d’autres traitements médicaux.
L’outil, appelé Deep Predictor of Binding Specificity (DeepPBS), est un modèle d’apprentissage profond géométrique conçu pour prédire la spécificité de liaison protéine-ADN à partir de structures complexes protéine-ADN. DeepPBS permet aux scientifiques et aux chercheurs de saisir la structure de données d’un complexe protéine-ADN dans un outil de calcul en ligne.
« Les structures des complexes protéine-ADN contiennent des protéines qui sont généralement liées à une seule séquence d’ADN. Pour comprendre la régulation des gènes, il est important d’avoir accès à la spécificité de liaison d’une protéine à n’importe quelle séquence d’ADN ou région du génome », a déclaré Remo Rohs, professeur et président fondateur du département de biologie quantitative et computationnelle du USC Dornsife College of Letters, Arts and Sciences.
« DeepPBS est un outil d’IA qui remplace le besoin de séquençage à haut débit ou d’expériences de biologie structurelle pour révéler la spécificité de la liaison protéine-ADN. »
L’IA analyse et prédit les structures protéines-ADN
DeepPBS utilise un modèle d’apprentissage profond géométrique, un type d’approche d’apprentissage automatique qui analyse les données à l’aide de structures géométriques. L’outil d’IA a été conçu pour capturer les propriétés chimiques et les contextes géométriques de la protéine-ADN afin de prédire la spécificité de liaison.
À l’aide de ces données, DeepPBS produit des graphiques spatiaux qui illustrent la structure des protéines et la relation entre les représentations des protéines et de l’ADN. DeepPBS peut également prédire la spécificité de liaison entre différentes familles de protéines, contrairement à de nombreuses méthodes existantes qui se limitent à une seule famille de protéines.
« Il est important pour les chercheurs de disposer d’une méthode qui fonctionne universellement pour toutes les protéines et qui ne se limite pas à une famille de protéines bien étudiée. Cette approche nous permet également de concevoir de nouvelles protéines », a déclaré Rohs.
Une avancée majeure dans la prédiction de la structure des protéines
Le domaine de la prédiction de la structure des protéines a connu des progrès rapides depuis l’avènement d’AlphaFold de DeepMind, qui permet de prédire la structure des protéines à partir de la séquence. Ces outils ont permis d’accroître les données structurelles disponibles pour les scientifiques et les chercheurs à des fins d’analyse. DeepPBS fonctionne en conjonction avec des méthodes de prédiction de structure pour prédire la spécificité des protéines sans structures expérimentales disponibles.
Rohs a déclaré que les applications de DeepPBS sont nombreuses. Cette nouvelle méthode de recherche pourrait accélérer la conception de nouveaux médicaments et traitements pour des mutations spécifiques dans les cellules cancéreuses, ainsi que conduire à de nouvelles découvertes en biologie synthétique et à des applications dans la recherche sur l’ARN.
Plus d’informations :
Raktim Mitra et al., Apprentissage profond géométrique de la spécificité de liaison protéine-ADN, Méthodes de la nature (2024). DOI: 10.1038/s41592-024-02372-w
Fourni par l’Université de Californie du Sud
Citation:Les chercheurs développent un modèle d’IA qui prédit la précision de la liaison protéine-ADN (2024, 9 août) récupéré le 9 août 2024 à partir de
Ce document est soumis au droit d’auteur. En dehors de toute utilisation équitable à des fins d’étude ou de recherche privée, aucune partie ne peut être reproduite sans autorisation écrite. Le contenu est fourni à titre d’information uniquement.
