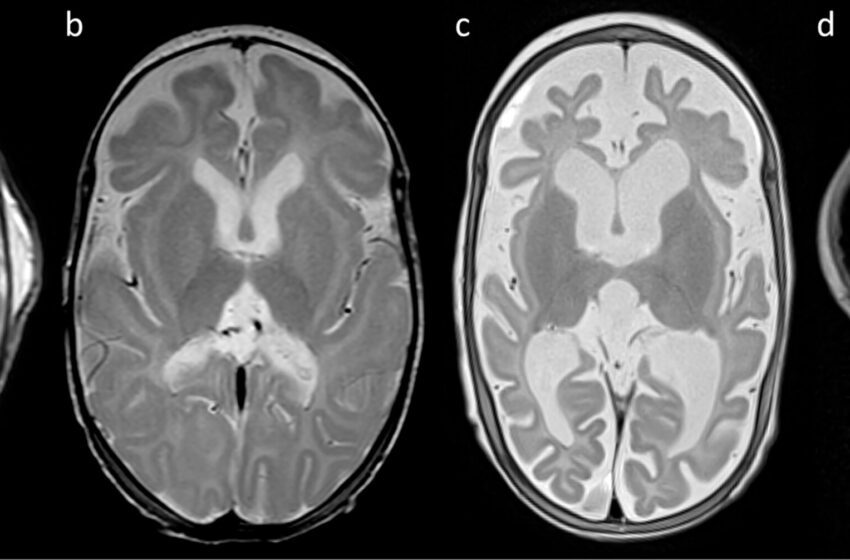
Le nourrisson prématuré souffrant de crises résistantes au médicament répond au traitement antisens en oligonucléotide
CMRI à l’âge de 5 semaines (a), 17 semaines (b) et 36 semaines (C et D). Crédit: Médecine de la nature (2025). Doi: 10.1038 / s41591-025-03656-0
Les chercheurs dirigés par Ludwig-Maximilians-Universität München ont induit une réduction supérieure à 60% de la fréquence des crises chez un nourrisson prématuré avec une encéphalopathie de développement et d’épileptique SCN2A à début précoce (DEE). Les crises se sont initialement produites à un rythme de 20 à 25 de l’heure et ont baissé de cinq à sept par heure après le dosage intrathécal répété avec Elsunersen, une thérapie oligonucléotide antisens.
Scn2a est un gène qui code pour le canal sodique de tension NAV1.2, qui est principalement exprimé dans les neurones excitateurs du système nerveux central. Ce canal joue un rôle clé dans la génération et la propagation potentielles d’action. Les variantes de SCN2A sont associées à un large spectre de troubles neurodéveloppementaux, selon que la variante entraîne une perte de fonction ou un effet de gain de fonction.
Les mutations de perte de fonction dans SCN2A sont liées à l’épilepsie avec un début ultérieur et, dans certains cas, aux troubles du spectre autistique sans crises. Les variantes de gain de fonction sont associées à des phénotypes plus graves, y compris des encéphalopathies de développement et d’épileptique à début précoce (DEE).
Dans ces cas, les convulsions commencent généralement au cours des trois premiers mois de la vie et s’accompagnent de retards de développement importants. Les bloqueurs de canaux sodiques peuvent réduire la fréquence des crises, mais offrent généralement un avantage limité au développement cognitif ou moteur.
Les oligonucléotides antisens (ASOS) sont de courtes volets d’acide nucléique conçues pour se lier à des cibles d’ARN spécifiques et réduire l’expression des gènes. Les ASO sont devenus une classe thérapeutique recherchée prometteuse pour cibler des mécanismes génétiques spécifiques.
Des études précliniques utilisant des modèles de gain de fonction SCN2A ont montré que les ASOS peuvent réduire l’expression de l’ARNm de Scn2a et une charge de crise plus faible. Étant donné que le gène SCN2A est hautement sensible à la dose, une réduction ciblée nécessite un étalonnage minutieux pour éviter les effets néfastes du sous ou une surexpression.
Dans l’étude, «Traitement des oligonucléotides antisens chez un nourrisson prématuré atteint d’encéphalopathie SCN2A et de l’encéphalopathie épileptique» Médecine de la natureLes chercheurs ont effectué une intervention clinique à patient unique pour évaluer la sécurité et le potentiel thérapeutique d’Elsunersen, un oligonucléotide antisens Gapmer ciblant l’ARNm de SCN2A.
Le patient était une femme prématurée née à 29 semaines et quatre jours de gestation, diagnostiquée avec SCN2A-DEE à début précoce sur la base de la présentation clinique et des tests génétiques. Les crises ont commencé le premier jour postnatal et ont persisté malgré une combinaison de médicaments conventionnels sur les antiseize.
À 7 semaines, le traitement a commencé avec l’administration d’Elsunersen via la ponction lombaire, fournissant le médicament dans le liquide céphalorachidien entourant la moelle épinière.
Pour évaluer l’effet du médicament sur le dysfonctionnement des canaux sodiques, l’équipe a utilisé une modélisation structurelle informatique et des tests électrophysiologiques in vitro. Les enregistrements de tension-clamp et les protocoles de serrage de potentiel d’action dynamique ont confirmé l’inactivation des canaux altérés et une augmentation du courant de sodium persistant.
Modélisation pharmacocinétique A estimé la distribution et la rétention des médicaments dans le liquide céphalo-rachidien et les tissus cérébraux. La fréquence des crises et les réponses cliniques ont été suivies tout au long de la période de traitement.
L’activité de crise n’était initialement pas réactive à neuf médicaments antiséizés conventionnels différents, notamment le phénobarbital, le lévétiracétam, la phénytoïne et le midazolam. Huit jours après la première dose intrathécale d’Elsunersen, des ruptures intermittentes du statut épilepticus (plusieurs crises sans récupération entre les épisodes) ont été observées. Les doses ultérieures ont conduit à une fin complète du statut épileptique et à une réduction soutenue de la fréquence des crises.
En 12 semaines, le dosage cumulé a atteint 2,5 mg sur trois administrations. La fréquence des crises a diminué d’une moyenne de 19,7 par heure à 6,6 par heure, ce qui représente une réduction de 67%. Après sept doses totales au cours de la phase de traitement initiale, le dosage mensuel s’est poursuivi avec dix administrations supplémentaires de 8 mg. Le contrôle des crises est resté stable à cinq à sept par heure, notamment après la phénytoïne à l’âge de 14 mois.
Les parents ont signalé une augmentation de la gravité et de la fréquence des crises d’environ quatre à six semaines après chaque administration, un schéma étayé par la modélisation pharmacocinétique. Ces observations ont informé l’intervalle de dosage. Tout au long du cours de traitement, aucun événement indésirable grave ou grave n’a été signalé.
Les signes vitaux, les panneaux sanguins et les évaluations cardiaques n’ont montré aucune anomalie attribuable au traitement. Aucune hydrocéphalie ou des complications liées à l’oligonucléotide antisens n’a été observée.
Au cours du suivi final à 22 mois, la fréquence des crises est restée de cinq à sept par heure, avec un dosage mensuel en cours d’Elsunersen.
Les résultats suggèrent une relation causale entre les intervalles de dosage et le contrôle des crises, tels que soutenus par la modélisation pharmacocinétique et la récurrence des crises quatre à six semaines après l’administration. Les chercheurs proposent que le contrôle des crises puisse être maximisée en combinant un traitement ASO avec des bloqueurs de canaux sodiques pour moduler l’excitabilité neuronale.
Dans un cas où plusieurs thérapies conventionnelles ont échoué, le traitement avec Elsunersen a réussi. Des études précliniques avaient déjà établi une justification mécaniste pour cibler les transcrits SCN2A avec des oligonucléotides antisens, ce qui rend les résultats attendus et pourtant extraordinaires. En tant que cas unique, une évaluation plus large de la sécurité d’Elsunersen, des exigences de dosage et de la généralisation nécessitera des essais cliniques formels.
Plus d’informations:
Matias Wagner et al, traitement des oligonucléotides antisens chez un nourrisson prématuré avec une encéphalopathie de développement et d’épileptique SCN2A à début précoce, Médecine de la nature (2025). Doi: 10.1038 / s41591-025-03656-0
© 2025 Science X Réseau
Citation: Le nourrisson prématuré ayant des crises résistantes au médicament répond au traitement aux oligonucléotides antisens (2025, 5 mai) récupéré le 5 mai 2025 à partir de
Ce document est soumis au droit d’auteur. Outre toute émission équitable aux fins d’études privées ou de recherche, aucune pièce ne peut être reproduite sans l’autorisation écrite. Le contenu est fourni uniquement à des fins d’information.
