Les chercheurs identifient un « interrupteur » pour activer la mort des cellules cancéreuses
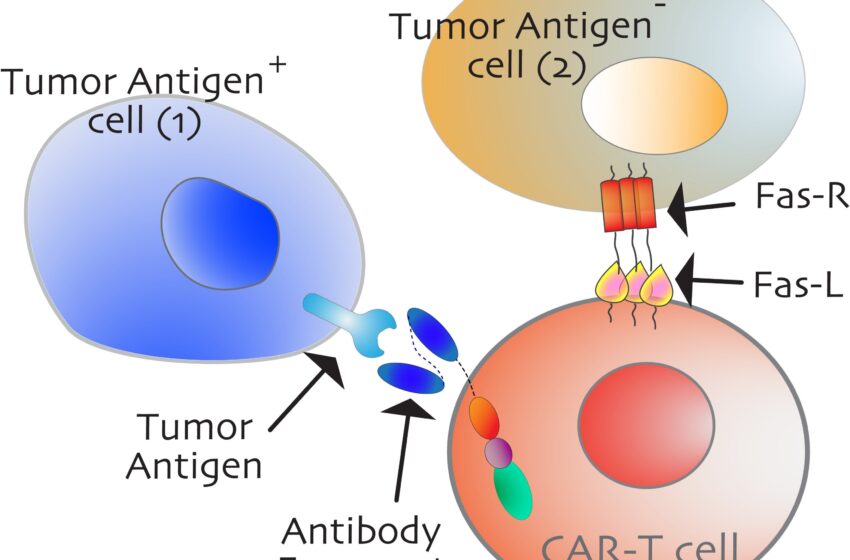
La cellule tumorale antigène-positive (bleue, à gauche) est une cible directe des cellules CAR-T (rouge clair) en raison des contacts anticorps-antigène de haute affinité. Au contraire, une cellule tumorale antigène négative (dorée claire, à droite) est tuée par l’assassinat de « spectateurs » médié par Fas. On s’attend à ce que les patients cancéreux présentant une expression élevée de Fas répondent nettement mieux aux immunothérapies. Crédit : UC Davis
Une équipe de recherche de l’UC Davis Comprehensive Cancer Center a identifié un épitope crucial (une section protéique qui peut activer la plus grosse protéine) sur le récepteur CD95 qui peut provoquer la mort des cellules. Cette nouvelle capacité à déclencher la mort cellulaire programmée pourrait ouvrir la porte à de meilleurs traitements contre le cancer. Les résultats ont été publiés le 14 octobre dans la revue Mort cellulaire et différenciation.
Les récepteurs CD95, également appelés Fas, sont appelés récepteurs de mort. Ces récepteurs protéiques résident sur les membranes cellulaires. Lorsqu’ils sont activés, ils libèrent un signal qui provoque l’autodestruction des cellules.
La modulation de Fas peut également étendre les avantages de la thérapie par cellules T du récepteur d’antigène chimérique (CAR) aux tumeurs solides comme le cancer de l’ovaire.
“Nous avons trouvé l’épitope le plus critique pour la signalisation cytotoxique du Fas, ainsi que pour la fonction antitumorale des lymphocytes CAR T”, a déclaré Jogender Tushir-Singh, professeur agrégé au Département de microbiologie médicale et d’immunologie et auteur principal de l’étude. .
“Les efforts précédents pour cibler ce récepteur ont échoué. Mais maintenant que nous avons identifié cet épitope, il pourrait y avoir une voie thérapeutique pour cibler Fas dans les tumeurs”, a déclaré Tushir-Singh.
Trouver de meilleurs traitements contre le cancer
Le cancer est généralement traité par chirurgie, chimiothérapie et radiothérapie. Ces traitements peuvent fonctionner au début, mais dans certains cas, les cancers résistants au traitement réapparaissent souvent. Les immunothérapies, telles que les thérapies immunitaires basées sur les cellules CAR T et les anticorps activant les molécules du récepteur du point de contrôle immunitaire, se sont révélées extrêmement prometteuses pour briser ce cycle. Mais ils n’aident qu’un très petit nombre de patients, notamment dans les tumeurs solides comme les cancers de l’ovaire, du sein triple négatif, du poumon et du pancréas.
Les lymphocytes T sont un type de cellules immunitaires. Les thérapies par cellules CAR T impliquent l’ingénierie des cellules T du patient en les greffant avec un anticorps spécifique ciblant la tumeur pour attaquer les tumeurs. Ces cellules T modifiées se sont révélées efficaces contre la leucémie et d’autres cancers du sang, mais n’ont pas réussi à plusieurs reprises à lutter contre les tumeurs solides. La raison en est que les microenvironnements tumoraux sont efficaces pour tenir à distance les cellules T et autres cellules immunitaires.
“On les appelle souvent tumeurs froides parce que les cellules immunitaires ne peuvent tout simplement pas pénétrer dans les microenvironnements pour produire un effet thérapeutique”, a déclaré Tushir-Singh. “Peu importe la façon dont nous concevons les anticorps activant les récepteurs immunitaires et les cellules T s’ils ne peuvent pas se rapprocher des cellules tumorales. Par conséquent, nous devons créer des espaces pour que les cellules T puissent s’infiltrer.”
Les récepteurs de mort font exactement ce que leur nom l’indique : lorsqu’ils sont ciblés, ils déclenchent la mort cellulaire programmée des cellules tumorales. Ils offrent une solution de contournement potentielle qui pourrait simultanément tuer les cellules tumorales et ouvrir la voie à des immunothérapies et à une thérapie par cellules CAR T plus efficaces.
Le développement de médicaments qui stimulent l’activité des récepteurs de la mort pourrait constituer une arme importante contre les tumeurs. Cependant, bien que les sociétés pharmaceutiques aient connu un certain succès en ciblant le Death Receptor-5, aucun agoniste du Fas n’a fait l’objet d’essais cliniques. Ces résultats pourraient potentiellement changer cela.
La bonne cible
Alors que Fas joue un rôle essentiel dans la régulation des cellules immunitaires, Tushir-Singh et ses collègues savaient qu’ils pourraient peut-être cibler les cellules cancéreuses de manière sélective s’ils trouvaient le bon épitope. Après avoir identifié cet épitope spécifique, lui et d’autres chercheurs peuvent désormais concevoir une nouvelle classe d’anticorps pour se lier sélectivement et activer Fas afin de potentiellement détruire spécifiquement les cellules tumorales.
D’autres recherches sur des modèles animaux et des essais cliniques sur l’homme ont montré que la signalisation Fas est fondamentale au succès du CAR T, en particulier dans les tumeurs génétiquement hétérogènes. Les tumeurs génétiquement hétérogènes contiennent un mélange de différents types de cellules, qui peuvent réagir différemment au traitement.
Un agoniste de Fas pourrait générer un effet spectateur CAR-T, dans lequel le traitement détruit les cellules cancéreuses dépourvues de la molécule pour laquelle l’anticorps ciblant la tumeur est conçu. En d’autres termes, l’activation de Fas peut détruire les cellules cancéreuses et améliorer l’efficacité du CAR T, un double coup de poing potentiel contre les tumeurs.
En fait, l’étude a montré que les tumeurs présentant une version mutée de l’épitope des récepteurs Fas ne répondraient pas du tout au CAR T. Cette découverte pourrait conduire à de nouveaux tests pour identifier les patients qui bénéficieront le plus de l’immunothérapie par cellules CAR-T.
“Nous devrions connaître le statut Fas d’un patient, en particulier les mutations autour de l’épitope découvert, avant même d’envisager de lui administrer CAR T”, a déclaré Tushir-Singh. “Il s’agit d’un marqueur définitif de l’efficacité du traitement par des tiers de la thérapie CAR T. Mais plus important encore, cela ouvre la voie au développement d’anticorps qui activent Fas, tuent sélectivement les cellules tumorales et soutiennent potentiellement la thérapie par cellules CAR T dans les tumeurs solides.”
Les autres auteurs incluent Tanmoy Mondal, Himanshu Gaur, Brice EN Wamba, Abby Grace Michalak, Camryn Stout, Matthew R. Watson, Sophia L. Aleixo, Arjun Singh, Roland Faller, Gary Scott Leiserowitz et Sanchita Bhatnagar de l’UC Davis. et Salvatore Condello de la faculté de médecine de l’Université d’Indiana.
Plus d’information:
Tanmoy Mondal et al, Caractérisation de l’épitope régulateur Fas (CD95) essentiel au ciblage des anticorps agonistes et à la fonction de spectateur CAR-T dans le cancer de l’ovaire, Mort cellulaire et différenciation (2023). DOI : 10.1038/s41418-023-01229-7
Citation: Des chercheurs identifient un « interrupteur » pour activer la mort des cellules cancéreuses (24 octobre 2023) récupéré le 24 octobre 2023 sur
Ce document est soumis au droit d’auteur. En dehors de toute utilisation équitable à des fins d’étude ou de recherche privée, aucune partie ne peut être reproduite sans autorisation écrite. Le contenu est fourni seulement pour information.
