Un nouveau système peut augmenter ou diminuer l’expression des gènes synthétiques
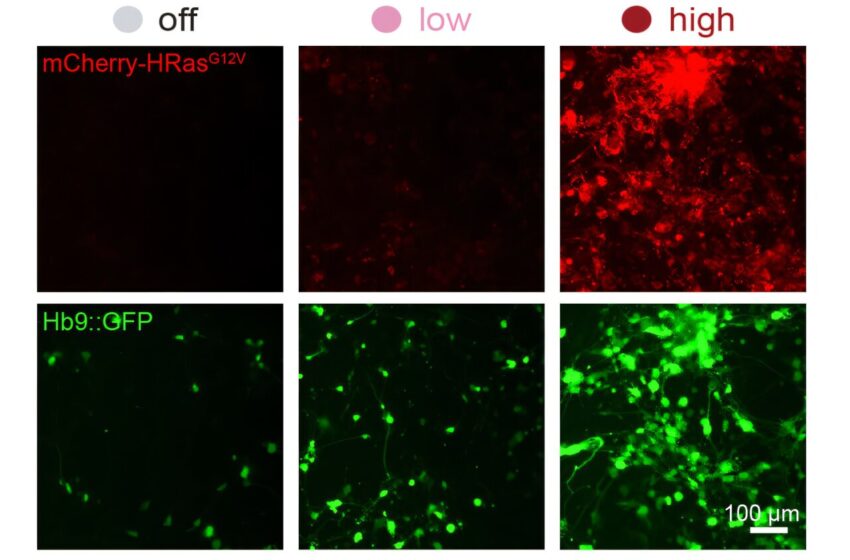
Les ingénieurs du MIT ont développé un moyen de définir les niveaux d’expression des gènes sur désactivé, faible ou élevé. En utilisant des cellules de la peau, les chercheurs ont créé un cocktail (marqué avec une protéine fluorescente rouge, rangée du haut) qui stimule la conversion des cellules de la peau en motoneurones. Via l’édition du promoteur, ils montrent que des niveaux plus élevés de ce cocktail augmentent le nombre de motoneurones (vert). Dans la rangée du bas, les mêmes cellules sont marquées avec une protéine fluorescente verte générée après la conversion des cellules en motoneurones. Crédit: Biotechnologie naturelle (2025). DOI : 10.1038/s41587-025-02854-y
Depuis des décennies, les biologistes synthétiques développent des circuits génétiques pouvant être transférés dans des cellules pour des applications telles que la reprogrammation d’une cellule souche en neurone ou la génération d’une protéine qui pourrait aider à traiter une maladie telle que le syndrome de l’X fragile.
Ces circuits génétiques sont généralement introduits dans les cellules par des porteurs tels que des virus non pathogènes. Cependant, il a été difficile de garantir que ces cellules finissent par produire la quantité correcte de protéine codée par le gène synthétique.
Pour surmonter cet obstacle, les ingénieurs du MIT ont conçu un nouveau mécanisme de contrôle qui leur permet d’établir un niveau de protéine souhaité, ou un point de consigne, pour n’importe quel circuit génétique. Cette approche leur permet également de modifier le point de consigne après la livraison du circuit.
“Il s’agit d’un outil vraiment stable et multifonctionnel. L’outil est très modulaire, vous pouvez donc contrôler de nombreux transgènes avec ce système”, explique Katie Galloway, professeur adjoint en génie chimique au MIT et auteur principal de la nouvelle étude.
En utilisant cette stratégie, les chercheurs ont montré qu’ils pouvaient inciter les cellules à générer des niveaux constants de protéines cibles. Dans une application qu’ils ont démontrée, ils ont converti des fibroblastes embryonnaires de souris en motoneurones en délivrant des niveaux élevés d’un gène qui favorise cette conversion.
Sneha Kabaria, étudiante diplômée du MIT, est l’auteur principal de l’article, publié aujourd’hui dans Biotechnologie naturelle. D’autres auteurs incluent Yunbeen Bae ’24 ; Mary Ehmann, Brittany Lende-Dorn, Emma Peterman et Kasey Love, étudiantes diplômées du MIT ; Adam Beitz Ph.D. ’25 ; et l’ancien postdoctorant du MIT Deon Ploessl.
Augmenter l’expression des gènes
Les circuits génétiques synthétiques sont conçus pour inclure non seulement le gène d’intérêt, mais également une région promotrice. Sur ce site, des facteurs de transcription et d’autres régulateurs peuvent se lier, activant ainsi l’expression du gène synthétique.
Cependant, il n’est pas toujours possible d’amener toutes les cellules d’une population à exprimer le gène souhaité à un niveau uniforme. L’une des raisons à cela est que certaines cellules peuvent n’occuper qu’une seule copie du circuit, tandis que d’autres en reçoivent beaucoup plus. De plus, les cellules présentent des variations naturelles dans la quantité de protéines qu’elles produisent.
Cela a rendu la reprogrammation des cellules difficile car il est difficile de garantir que chaque cellule d’une population de cellules cutanées, par exemple, produira suffisamment de facteurs de transcription nécessaires pour réussir la transition vers une nouvelle identité cellulaire, comme un neurone ou une cellule souche pluripotente induite.
Dans le nouvel article, les chercheurs ont conçu un moyen de contrôler les niveaux d’expression des gènes en modifiant la distance entre le gène synthétique et son promoteur. Ils ont découvert que lorsqu’il y avait un « espaceur » d’ADN plus long entre la région promotrice et le gène, le gène serait exprimé à un niveau inférieur. Cette distance supplémentaire, ont-ils montré, rend moins probable que les facteurs de transcription liés au promoteur activent efficacement la transcription des gènes.
Ensuite, pour créer des points de consigne pouvant être modifiés, les chercheurs ont incorporé des sites dans l’espaceur qui peuvent être excisés par une enzyme appelée Cre recombinase. Lorsque des parties de l’espaceur sont découpées, cela contribue à rapprocher les facteurs de transcription du gène d’intérêt, ce qui entraîne l’expression du gène.
Les chercheurs ont montré qu’ils pouvaient créer des espaceurs dotés de plusieurs points d’excision, chacun ciblé par des recombinases différentes. Cela leur a permis de créer un système appelé DIAL, qu’ils pourraient utiliser pour établir des points de consigne « élevés », « moyens », « bas » et « off » pour l’expression des gènes.
Une fois le segment d’ADN portant le gène et son promoteur délivré dans les cellules, des recombinases peuvent être ajoutées aux cellules, permettant ainsi de modifier le point de consigne à tout moment.
Les chercheurs ont démontré leur système dans des cellules de souris et humaines en délivrant le gène de différentes protéines fluorescentes et gènes fonctionnels, et ont montré qu’ils pouvaient obtenir une expression uniforme dans une population de cellules au niveau cible.
“Nous avons obtenu un contrôle uniforme et stable. C’est très excitant pour nous car le manque de contrôle uniforme et stable est l’une des choses qui limitent notre capacité à construire des systèmes fiables en biologie synthétique. Lorsqu’il y a trop de variables qui affectent votre système, et que vous ajoutez ensuite une variation biologique normale, il est très difficile de construire des systèmes stables”, explique Galloway.
Reprogrammation des cellules
Pour démontrer les applications potentielles du système DIAL, les chercheurs l’ont ensuite utilisé pour délivrer différents niveaux du gène HRas.G12V aux fibroblastes embryonnaires de souris. Il a déjà été démontré que cette variante HRas augmente le taux de conversion des fibroblastes en neurones. L’équipe du MIT a découvert que dans les cellules ayant reçu une dose plus élevée du gène, un plus grand pourcentage d’entre elles étaient capables de se transformer avec succès en neurones.
Grâce à ce système, les chercheurs espèrent désormais réaliser des études plus systématiques sur différents facteurs de transcription pouvant induire la transition des cellules vers différents types de cellules. De telles études pourraient révéler comment différents niveaux de ces facteurs affectent le taux de réussite et si la modification des niveaux de facteurs de transcription pourrait modifier le type de cellule généré.
Dans le cadre de travaux en cours, les chercheurs ont montré que DIAL peut être combiné avec un système qu’ils ont développé précédemment, connu sous le nom de ComMAND, qui utilise une boucle de rétroaction pour empêcher les cellules de surexprimer un gène thérapeutique.
En utilisant ces systèmes ensemble, il pourrait être possible d’adapter les thérapies géniques pour produire des niveaux de protéines spécifiques et cohérents dans les cellules cibles de chaque patient, affirment les chercheurs.
“C’est quelque chose qui nous passionne car DIAL et ComMAND sont hautement modulaires, de sorte que vous pourriez non seulement avoir une thérapie génique bien contrôlée qui soit quelque peu générale pour une population, mais vous pourriez, en théorie, l’adapter à n’importe quelle personne ou à n’importe quel type de cellule donné”, explique Galloway.
Plus d’informations :
Sneha R. Kabaria et al, Édition de promoteurs programmables pour un contrôle précis de l’expression du transgène, Biotechnologie naturelle (2025). DOI : 10.1038/s41587-025-02854-y
Fourni par le Massachusetts Institute of Technology
Cette histoire est republiée avec l’aimable autorisation de MIT News (web.mit.edu/newsoffice/), un site populaire qui couvre l’actualité de la recherche, de l’innovation et de l’enseignement du MIT.
Citation: Un nouveau système peut augmenter ou diminuer l’expression de gènes synthétiques (13 octobre 2025) récupéré le 13 octobre 2025 sur
Ce document est soumis au droit d’auteur. En dehors de toute utilisation équitable à des fins d’étude ou de recherche privée, aucune partie ne peut être reproduite sans autorisation écrite. Le contenu est fourni à titre informatif uniquement.
