Développer une méthode simple et rentable pour identifier les cibles d’une enzyme cruciale de modification des protéines
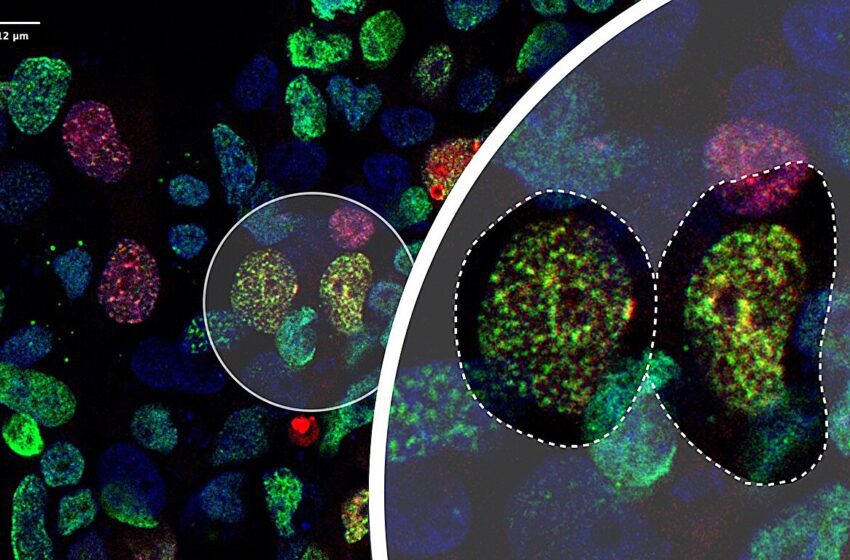
L’application de la technologie Ub-POD à l’ubiquitine ligase RAD18 permet de visualiser les points chauds de réparation des dommages à l’ADN induits par les UV dans les cellules humaines. Crédit : Urbi Mukhopadhyay/EMBL, Isabel Romero Calvo/EMBL
Les protéines humaines subissent une variété de modifications chimiques après leur synthèse. Ces modifications régulent leur structure, leur fonction et leur stabilité. Des chercheurs du groupe Bhogaraju de l’EMBL Grenoble ont développé une nouvelle méthode pour étudier un type critique de processus de modification des protéines appelé ubiquitination. L’ubiquitination joue un rôle essentiel dans diverses fonctions cellulaires et sa dérégulation contribue à de nombreuses maladies humaines, notamment la neurodégénérescence et le cancer.
Lors de l’ubiquitination, un groupe d’enzymes appelés ubiquitine ligases E3 fixe une petite protéine appelée ubiquitine à d’autres protéines. Ce marquage, à son tour, aide à déterminer le sort de la protéine ciblée. L’ubiquitination est très répandue chez l’homme et on estime que chaque protéine humaine subit une ubiquitination au moins une fois dans sa vie.
La diversité des fonctions cellulaires de l’ubiquitination se reflète dans l’existence de plus de 600 gènes de ligase E3 humains, représentant environ 3 % du génome humain. La cartographie du paysage des protéines cibles E3 humaines peut nous aider à comprendre leur fonction et éventuellement à les cibler à des fins thérapeutiques.
Cependant, un nombre significatif de ligases E3 et de leurs cibles restent mal caractérisées, l’une des raisons étant la nature extrêmement transitoire de leur interaction. Les méthodes actuelles de cartographie de ces interactions nécessitent également beaucoup de ressources, ce qui limite leur utilisation et leur évolutivité.
Pour résoudre ce problème, le groupe Bhogaraju, qui étudie les voies d’ubiquitination dans divers contextes physiologiques, a développé une méthode simple et rentable, appelée Ub-POD, pour étiqueter rapidement et facilement les cibles d’une enzyme ligase E3 donnée directement dans les cellules humaines.
L’ouvrage, qui a été récemment publié dans la revue Progrès scientifiquesa été dirigé par Urbi Mukhopadhyay, un chercheur postdoctoral EMBO du groupe Bhogaraju, qui a trouvé un moyen d’étiqueter efficacement les cibles ubiquitinées d’une ligase E3 donnée avec de la biotine directement à l’intérieur des cellules. Cela permet d’identifier ultérieurement les cibles à l’aide d’une technique appelée spectrométrie de masse quantitative. La biotine est un petit composé organique qui peut être fixé biochimiquement aux protéines d’intérêt et utilisé pour les isoler d’un échantillon mixte.
La simplicité de la méthode et l’utilisation de produits chimiques courants signifient qu’elle peut être utilisée partout dans le monde, dans n’importe quel laboratoire doté d’installations de biologie moléculaire de base.
En utilisant cette méthode et en guise de preuve de principe, les chercheurs ont identifié de nouvelles cibles des ligases E3, RAD18 et CHIP, impliquées respectivement dans le cancer et les maladies neurodégénératives. Le laboratoire de Christian Behrend à l’Université Ludwig-Maximilians (LMU) de Munich, qui collabore avec le groupe Bhogaraju, a également appliqué cette méthode à TRAF6, une autre ligase E3 et un régulateur essentiel de la signalisation immunitaire, et a identifié avec succès des substrats connus et nouveaux.
À l’avenir, l’équipe prévoit d’appliquer cette méthode à toutes les enzymes E3 humaines connues.
« Nous pensons que cela contribuera à combler la disparité dans l’espace thérapeutique entre la famille des protéines kinases et la famille des ubiquitines ligases », a déclaré Sagar Bhogaraju, chef de groupe à l’EMBL Grenoble. « Bien qu’ils hébergent un nombre similaire d’enzymes, il existe environ 80 agents thérapeutiques approuvés par la FDA qui ciblent les kinases, tandis que seule une poignée de médicaments ciblent le système ubiquitine. La méthode que nous avons développée contribuerait à élargir le champ d’application des ligases E3 ou de leurs substrats en tant que cibles médicamenteuses. »
Plus d’informations :
Urbi Mukhopadhyay et al, Une approche d’étiquetage spécifique à l’ubiquitine basée sur la proximité pour l’identification des substrats de l’ubiquitine ligase, Progrès scientifiques (2024). DOI: 10.1126/sciadv.adp3000
Fourni par le Laboratoire européen de biologie moléculaire
Citation:Développement d’une méthode simple et rentable pour identifier les cibles d’une enzyme cruciale de modification des protéines (2024, 12 août) récupéré le 12 août 2024 à partir de
Ce document est soumis au droit d’auteur. En dehors de toute utilisation équitable à des fins d’étude ou de recherche privée, aucune partie ne peut être reproduite sans autorisation écrite. Le contenu est fourni à titre d’information uniquement.
